Cinética química
Los objetivos de estudios de la
cinética química son la determinación de la
rapidez de las reacciones y su dependencia con algunos
parámetros tales como concentración, temperatura y
catalizadores, así la compresión del mecanismo de
reacciones, es decir el número de etapas involucradas y la
naturaleza de los intermediarios que se forman.
El tema de la cinética
química es, conceptualmente, más sencillo de
entender que algunos otros temas de la físico
química, como la termodinámica y la mecánica
cuántica, a pesar de que el tratamiento teórico
riguroso de la energética involucrada solo es posible en
el caso de sistemas muy sensibles en fase gaseosa. No obstante,
el enfoque microscópico empírico puede proporcionar
mucha información útil

Usos de la
cinética química:
La cinética se puede aplicar a la
optimización de las condiciones de un proceso, por
ejemplo
En la síntesis en química
orgánica, en reacciones analíticas y en la
manufactura química. Adicionalmente, otro uso
práctico de la cinética es la determinación
y control de la estabilidad de los productos comerciales,
farmacéuticos, pinturas
El estudio de los mecanismos de
reacción:
Definición de mecanismo de
reacción. La siguiente reacción hipotética
en un paso a paso:
AB + C ———- A + BC
Los componentes del lado izquierdo son los
reactivos, no se transforman inmediatamente en productos; los
productos presentan cierta estabilidad. Esta resistente a que
sucedan las reacciones químicas se debe a la
energía necesaria para pasar de reactivos a productos.
Podemos imaginar que el sistema reacciona o sigue una trayectoria
y que pasa a través de un máximo que se encuentra
en algún lado entre los estados inicial o
final.

Un mecanismo de reacción postulado
es una descripción de todas las reacciones elementales que
contribuyen (a esto lo llamamos esquema cinético),
así como de una descripción de las estructuras
(electrónicas y químicas) y la
estereoquímica del estado de transición para cada
reacción elemental.
Ejemplo, hidrólisis alcalina de un
éster:
RCOOR"+ OH-?RCOO-+ R"OH
Muchos estudios experimentales sugieren que
se trata de una reacción compleja. Los pasos esenciales se
muestran en el siguiente esquema cinético:
RCOOR"+ OH-?I 1)
I ?RCOOH + R"O-2)
Una tercera reacción rápida,
transferencia de protones genera concentraciones de equilibrio
entre RCOO-+ R"OH.I representa un intermediario cuya estructurase
muestra a continuación: Esta descripción nos
proporciona información, mediante estructuras
convencionales, acerca de la constitución de los
reactivos, productos e intermediario.
Es posible intentar mostrar una
distribución y flujo de electrones del estado de
transición. Sin embargo, debe tomarse en cuenta que se
puede tener una idea burda de la distribución
electrónica en esta especie siempre que se cumpla con los
requisitos de que las cargas parciales deben igualar la suma de
carga correctamente, lo mismo que los enlaces
parciales
En un nivel más profundo, el
mecanismo de reacción requiere de un tratamiento
cuantitativo de los cambios energéticos en la trayectoria
de la reacción y una descripción mecánica
cuántica de la estructura del estado de
transición.
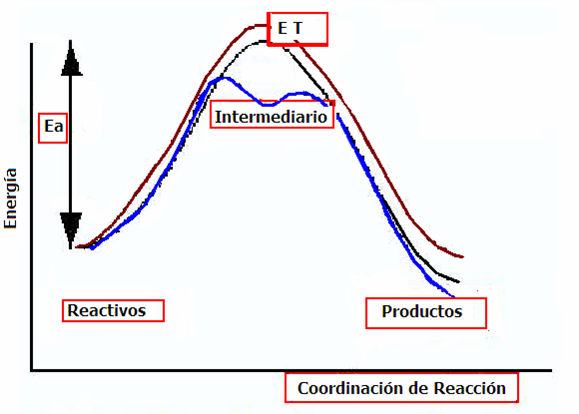
Coordenada de reacción

En el proceso de establecer el esquema
cinético, los estudios de velocidad determinan los efectos
de las diversas variables posibles: temperatura, presión,
concentraciones de los reactivos, fuerza iónica,
disolvente y efectos de las superficies
CINÉTICA
QUÍMICA EXPERIMENTAL
Las velocidades de
reacción
Nos referiremos básicamente a
sistemas cerrados, es decir, aquellos en los que ni se gana ni se
pierde materia durante el periodo de
observación.
La ecuación (1) representa cualquier
reacción química balanceada, Ai representa
reactivos y productos, Vi es negativo para reactivos y positivo
para productos.

(1)
Gráficas de concentración
en función del tiempo para reacciones de
a)Orden cero
b)Orden uno
c)Orden dos
Gráfico de orden cero: la rapidez
es independiente de la concentración:

Una gráfica de [A] contra tiempo
da una línea recta cuya pendiente es k y el valor de la
ordena da al origen es [A]0.
Reacciones de primer
orden.
Una reacción de primer orden es
aquélla en la que la velocidad de reacción depende
únicamente de un reactivo. Por ejemplo, la
isomerización de isocianuro de metilo,
CH3NC:
CH3NC ?CH3CN
Una reacción de primer orden es
aquella en la que la rapidez de la raccion depende solo de la
concentración de reactivo, elevada a la primera
potencia
Rapidez = –d[A] / dt
=k[A]
Reacción de segundo
orden:
Hay dos casos de cinéticas de
segundo orden. El primer caso es una reacción entre dos
especies idénticas:
A + A
?productos
la expresión de velocidad para
este caso es:(22)
El segundo caso es una reacción
global de segundo orden entre dos especies
diferentes
:[]2][21AkdtAdv=-
Autor:
Quispe Pacori, Esthefany
Victoria
Mamani Prado; Edith
Katherine
UNIVERSIDAD ANDINA NESTOR CACERES
VELASQUEZ
CARRERA ACADEMICO PROFESIONAL
FARMACIA Y BIOQUIMICA