La presencia de larvas de anisákidos en
músculo de pescado eviscerado se debe a la
migración post-mortem. Por tanto, es imprescindible que el
tiempo que transcurre entre la captura y la evisceración
sea mínimo (EFSA, 1998). La mayor incidencia y
número de larvas se detectan en la musculatura hipoaxial.
Por ello, la eliminación de esta parte (ventresca o ijada)
en las especies que más frecuentemente están
infestadas, contribuye a disminuir el riesgo (JEMMI et al., 2000;
FDA, 2001; HUSS et al., 2003).
La congelación rápida con aire "blast
freezing" o túneles de congelación rápida en
el buque es un método eficaz de inactivar las larvas de
anisákidos aunque es probable que no destruya la capacidad
de sensibilización de los antígenos de la larva
(EFSA, 1998).
c. Manipulación en Tierra e
Inspección
Si no se ha llevado a cabo en el buque, debe procederse
a la evisceración y lavado de la cavidad abdominal lo
más rápidamente posible tras el desembarque y, si
es posible, eliminación de la musculatura hipoaxial. Esto
último tiene inconvenientes si se va a comercializar
entero ya que en general tiene poca aceptación por parte
del consumidor y siempre supone una pérdida de casi el 15%
(JEMMI et al., 2000; HUSS et al., 2003).
Al pescado eviscerado se le debe realizar un examen
visual de la cavidad abdominal, hígado y lechazas
destinadas al consumo humano (FDA, 2001).
En el caso de filetes, se realiza examen visual de un
número representativo de la partida. El examen se realiza
en la superficie y se eliminan las larvas con un cuchillo (HUSS
et al., 2003). Para detectar las larvas en la profundidad del
músculo, se debe practicar un examen por
transiluminación.
En esta fase, la evisceración, la
inspección visual, la eliminación física de
las larvas y la exclusión de la musculatura hipoaxial
pueden reducir el peligro asociado a anisákidos,
pero no lo eliminan ni lo reducen hasta un nivel aceptable. Por
ello, es necesario congelar previamente los productos que se van
a consumir crudos o poco procesados.
d. Productos de la Pesca Procesados
Tratamiento térmico del pescado destinado a
ser comido cocinado
Las larvas de anisákidos son sensibles al calor.
Se ha demostrado que las larvas en el tejido muscular de los
peces se inactivan en un tiempo de 5 a 10 minutos al someter los
pescados a tratamientos térmicos en los que se alcancen
temperaturas superiores a 60º C en el centro del producto.
El tiempo necesario variará en función del proceso
culinario y, especialmente, del tamaño de las piezas. Por
ello, es más seguro el cocinado de aquellas más
pequeñas (AZTI-TECNALIA, 2004).
Para comprobar que se ha alcanzado la temperatura
mínima necesaria, en restauración está
especialmente indicado el uso de termómetros de cocina
(termómetros especiales para alimentos).
Por lo tanto, son seguros, desde el punto de vista de la
inactivación del parásito, los productos cocinados
completamente, es decir, hervidos y fritos, dado que en tales
tratamientos se alcanzan temperaturas superiores a los 90 y
170º C, respectivamente. Además los productos
cocinados a la plancha, siempre y cuando se verifique que el
pescado está completamente cocido. Ayuda al proceso que la
plancha esté caliente al comienzo y las piezas se volteen
durante el cocinado. Para asegurarse de que el tratamiento es
eficaz y que se ha alcanzado una temperatura mínima de
60º C, se puede pinchar con un tenedor o cuchillo y
comprobar que la carne se separa sin dificultad de la espina y
que posee un aspecto mate típico de las proteínas
coaguladas.
En el caso del cocinado en microondas se deben
garantizar las condiciones mínimas de temperatura y
tiempo, se tome la precaución de dar una o dos vueltas al
pescado durante la cocción para eliminar puntos
fríos y, una vez cocinado, se deje reposar la pieza
cubierta durante, al menos, dos minutos para permitir que la
temperatura se distribuya de forma homogénea por el
producto, ya que las microondas a alcanzan un determinado espesor
en el alimento y el resto del calentamiento se produce por
conducción (AESAN, 2005).
En la tabla 2 se muestran los resultados de un estudio
con filetes de pescado (166-467 grs de peso y 0,5-1,75 cm de
grosor) calentados en un microondas de 700W al máximo de
potencia (ADAM et al., 1999).
TEMPERATURA DE TRATAMIENTO | SUPERVIVENCIA (%) |
60 | 31 |
65 | 11 |
71 | 2 |
77 | 0 |
Tabla 2. Supervivencia de las larvas
de Anisakis simplex a un tratamiento con
microondas.
Para procedimientos de cocinado en los que no se vayan a
alcanzar estas condiciones de temperatura y tiempo, será
necesario haber realizado una congelación previa en las
condiciones que se indican a continuación.
Tratamiento para el pescado a comer crudo o
prácticamente crudo: Congelación
La congelación es el método más
efectivo para el control y la prevención de la
anisakiasis, ya que produce la inactivación de las
larvas.
En la actualidad, la legislación europea y
nacional establece que, los productos de la pesca que vayan a ser
consumidos crudos o prácticamente crudos deberán
congelarse a una temperatura igual o inferior a –20º C
en la totalidad del producto, durante un período de, al
menos, 24 horas, en el producto bruto o acabado.
Es importante resaltar que la eficacia de la
congelación depende de la temperatura y tiempo en el
cuál se alcanza dicha temperatura, siendo de especial
relevancia en la restauración colectiva y en los hogares,
donde habitualmente no se emplean sistemas rápidos de
congelación. Por ello, se recomienda que la
congelación se lleve a cabo a temperatura igual o inferior
a –20º C durante siete días (FDA, 2001), con el
fin de garantizar la eficacia del tratamiento. Especialmente en
restauración colectiva se comprobará que se alcanza
esta temperatura en el compartimento congelador. Por otro lado,
en frigoríficos domésticos sin indicador de
temperatura debe tenerse en cuenta que la temperatura
mínima alcanzada, varía en función del
número de estrellas de los mismos. Así, un
frigorífico de una estrella podría alcanzar una
temperatura mínima de –6ºC, uno de dos
estrellas una temperatura mínima de –12º C, y
sólo los frigoríficos de tres estrellas, los
frigoríficos congeladores de cuatro estrellas, los
congeladores verticales y los congeladores tipo arcón
alcanzan temperaturas inferiores a los –18º
C.
Es por ello necesario, que los usuarios y consumidores
comprueben que la temperatura a la que está operando el
congelador del frigorífico, sea igual o inferior a
–20º C.
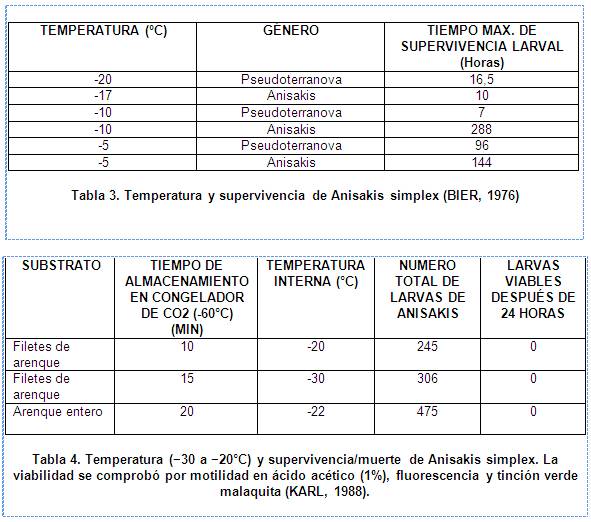
BIER (1976) y KARL (1988) presentaron los datos que se
detallan a continuación en las tablas 3 y 4, referentes a
los tiempos de supervivencia/muerte de Anisakis simplex sometidos
a temperaturas de congelación.
Acidificación
De los trabajos publicados se deduce que es necesaria la
congelación de pescados escabechados y marinados, ya que,
para la destrucción de las larvas se requiere mantener
durante 35 días una concentración del 2,5% de
ácido acético y 6% de NaCl (AESAN, 2005), ó
bien mantener al menos durante 13 días una
concentración del 6% de ácido acético y del
12% de sal (SÁNCHEZ et al., 2005).
Es por esto, que el método tradicional por el que
se elaboran los boquerones en vinagre, basado en la permanencia
de los mismos en vinagre comercial, con un contenido aproximado
del 6% de ácido acético, y sal durante 4 a 24
horas, resulta insuficiente para la inactivación de las
larvas de anisákidos.
Salazón
Aunque los anisákidos son sensibles a la sal se
necesitan elevadas concentraciones durante un período
prolongado para inactivar las larvas. Algunos datos sobre el
efecto del cloruro de sodio se recogen en la tabla 5.
% NaCl EN LA FASE ACUOSA DEL | TIEMPO MÁXIMO DE |
4-5 | 6 – > 17 semanas |
6-7 | 10–12 semanas |
8-9 | 5–6 semanas |
15 | 4 semanas |
20 | 3 semanas |
Tabla 5. Tiempo de supervivencia de
larvas de anisákidos en solución de NaCl (ICMSF,
1996; HUSS et al., 2003).
La salazón en seco inactiva las larvas de la
superficie pero, si no es prolongada, generalmente no inactiva
las del interior (FDA, 2001). La sacarosa también inactiva
al parásito pero se necesitan concentraciones del 12%
durante, al menos, 35 días (ICMSF, 1996).
Los pescados preparados en sal también requieren
de congelación, en función de la
concentración de sal alcanzada en el pescado, y del tiempo
que se mantenga dicha salazón. Sería necesario
realizar congelación en el caso de que la
concentración de NaCl en el pescado no alcance un nivel en
torno al 8 a 9% mantenida durante 6 semanas (AESAN, 2005). Por
esto, se debe prestar especial cuidado en el caso de los
denominados "pescado muy ligeramente salado" y "pescado
ligeramente salado" cuyos niveles de NaCl son inferiores al 10%
(CODEX ALIMENTARIUS, 2004).
No es necesario congelar los pescados salados cuando la
concentración de sal alcance niveles superiores al 9% de
NaCl y se mantenga así durante seis semanas. Las
semiconservas tradicionales de anchoas garantizan la
inactivación de la larva, ya que, el procedimiento se
lleva a cabo mediante la conservación en sal durante 5 a
12 meses, alcanzándose concentraciones superiores al 12%
de sal; tiempo y concentración superior a la requerida
para inactivar las larvas. Además, en procesos
tradicionales de salazón de arenques en los que se
alcanzan concentraciones de sal en el pescado de entre el 13% y
el 16% no es necesaria la congelación. Se ha comprobado
experimentalmente, con pescados parasitados, que al cabo 16
días de permanencia en la salazón resultaban
inactivadas todas las larvas de anisákidos (CEVPM,
2005).
No requieren ser congelados los "pescados medianamente
salados" (CODEX ALIMENTARIUS, 2004), lo cuales alcanzan
concentraciones de sal en el pescado que alcanzan niveles entre
el 10 % y el 20% de NaCl y se mantienen así durante cuatro
a cinco semanas y tampoco los "pescados muy salados" (CODEX
ALIMENTARIUS, 2004) que presentan concentraciones de sal que
alcanzan niveles al menos del 20% de NaCl y se mantienen
así durante tres semanas.
Conclusiones
De la revisión de la bibliografía
disponible se ha podido concluir lo siguiente:
1. La anisakiasis es una enfermedad de baja
prevalencia, pero emergente y de distribución mundial.
Está clasificada por la Unión Europea como una
enfermedad rara.2. En España se han descrito pocos casos
aún siendo uno de los mayores consumidores de pescado
por habitante en el mundo, lo cual probablemente se deba al
hecho de que el pescado se suele consumir
cocinado.3. A pesar del bajo porcentaje de
infestación por anisákidos, el boquerón
en vinagre y aceite parece ser la fuente principal de
transmisión de anisakiasis; aunque también se
han atribuido casos a la ingestión de sardinas y de
merluza por ser estos los productos del mar que más
frecuentemente se consumen crudos o poco
cocinados.4. Esta enfermedad produce un cuadro
clínico conocido, con sintomatología
gastrointestinal y/o alérgica, pero que puede
prevenirse fácilmente si se siguen las recomendaciones
dispuestas por AESAN para el consumidor de productos de la
pesca.5. Se ha demostrado la eficacia de varias
medidas de prevención de la anisakiasis, dentro de las
cuales la más efectiva es la congelación de los
productos de la pesca que vayan a ser consumidos crudos o
prácticamente crudos, a una temperatura igual o
inferior a –20º C durante al menos 24
horas.6. La normativa vigente tiene un doble enfoque,
por una parte, hacia la regulación y control de las
medidas de prevención a nivel de productores,
distribuidores y en el ámbito de la
restauración, y por otra parte, hacia la
educación de los consumidores.7. La evolución en las técnicas
de detección de las larvas en el pescado ha permitido
aumentar la sensibilidad en el diagnóstico, evitando
deteriorar la pieza examinada.
Bibliografía
ABOLLO, E; GESTAL, C; PASCUAL, S. 2001. Anisakis |
ADAM, A; MILLER, K; WEKELL, M; DONG, F. 1999. |
ADROHER, FJ; VALERO, A; RUIZ-VALERO, J; IGLESIAS, |
AESAN. 2005. Comité Científico de la |
AKAO, N; OHYAMA, T; KONDO, K. 1990. Immunoblot |
ALONSO, A; DASCHNER, A; MORENO, A. 1997. |
ALONSO-GOMEZ, A; MORENO-ANCILLO, A; LOPEZ-SERRANO, |
AÑIBARRO, B; SEOANE, F. 1998. Occupational |
ARENAL-VERA, J; MARCOS, J; BORREGO, M; BOWAKIN, W; |
ARMENTIA, A; LOMBARDERO, M; CALLEJO, A; MARTIN |
AUDICANA, M. 2002. Anisakis simplex y alergia |
AUDICANA, M; FERNÁNDEZ DE CORRES, L; |
AZTI-TECNALIA. 2004. Centro Tecnológico |
BAEZA, ML; ZUBELDIA, JM; RUBIO, M. 2001. Anisakis |
BIER, J.W. 1976. Experimental anisakiasis: |
BUENDIA, E. 2000. ¿Cuándo se |
CARRETERO, P; BLANCO, J; GARCÍA, F; MARCOS, |
CEVPM. 2005. Centre d´Experimentation et de |
CHENG, T.C. 1982. Anisakiasis. En: Handbook series |
CHODHURY, G; JENKS, W; WIRSWO, J; BUBLITZ, C. |
CODEX ALIMENTARIUS. 2004. Norma de Codex para el |
CUELLAR, M; FONTANILLAS, J; PÉREZ FUENTES, |
CUENDE, E. 1998. Rheumatic manifestations in the |
DASCHNER, A; ALONSO, G; MARKOMEZ, A; CABANAS, R; |
DASCHNER, A; ALONSO-GOMEZ, A; CABALLERO, T; 828. |
DASCHNNER, A; ALONSO GÓMEZ, A; MORA, C; |
DEL OLMO, M; COZAR, A; MARTÍNEZ, J. M.; |
DOMÍNGUEZ, J; CIMARRA, M; SEVILLA, M; |
DOMÍNGUEZ, J; |
EFSA. 1998. European Food Safety Authority, Veterinary Measures relating to Public Health – simplex antigens and evaluation of the possible Disponible en: |
ESPIÑEIRA, M; HERRERO, B; VIEITES, J.M; |
FALCAO, H; LUNET, N; NEVES, E; BARROS, H. 2002. Do |
FDA. 2001. Food and Drug Administration. Fish and |
FERNÁNDEZ CALDAS, E; QUIRCE, S; |
HUANG, W. 1990. Methodes de recherché de |
HUSS, H; ABABOUCH, L; GRAM, L. 2003. Assessment |
ICMSF. 1996. Microorganisms in Foods 5. Pathogens. Blackie Academic & Professional, |
JEMMI, T; SCHMITT, M; RIPPEN, T. 2000. Safe |
KARL, H. 1988. Untersuchungen zur |
KASUYA, S; HAMANO, H; IZUMI, S. 1990. Mackerel |
KIMURA, S; TAKAGI, Y; GOMI, K. 1999. IgE response |
LOPEZ GIMÉNEZ, R; CASTELL MONSALVE, J. |
LÓPEZ SABATER, E; LÓPEZ SABATER, C. |
LÓPEZ-SERRANO, M; ALONSO, A; DASCHNER, A; |
LOUREDO-MÉNDEZ, A; ACEDO DE LA ROSA, F; |
MATSUOKA, H; NAKAMA, T; KISANUTI, H; UNO, H; |
MINISTERIO DE LA PRESIDENCIA. Real Decreto |
MINISTERIO DE LA PRESIDENCIA. Real Decreto |
NOBORO, K; HIROSHI, I. 1992. A case of abdominal |
OLSON, A; LEWIS, M; HAUSER, M. 1983. Proper |
ORPHANET. 2010. Informes Periódicos, Mayo. |
OSANZ, AC. 2001. Tesis Doctoral: Presencia de |
OSHIMA, T. 1972. Anisakis and anisakiasis in Japan |
PELLOUX, H; PINEL, C; AMBROISE THOMAS, P. 1992. |
PEREIRA BUENO, J. 1992. Algunos aspectos de la |
PEREIRA, V; LEVI, A; BOAINAIN, E. 1989.
|
PÉREZ, A; MARTÍN, JL; PÉREZ, REGLAMENTO (CE) Nº 853/2004 del Parlamento |
ROMERO, JA; MARTÍNEZ, AE; OLIVARES, U; |
RUSHOVICH, A; RANDALL, E; CAPRINI, J; |
SÁNCHEZ, I; DE ARMAS, C; MARTÍNEZ, |
SHIRAHAMA, M; KOGA, T; ASHIBASHI, H; UCHIDA, S; |
SMITH, J.W. y WOOTTEN, R. 1978. Anisakis and |
TADAMORI, S; SHIGEYUKI, I; HISATO, H; TOMONORI, A; |
TRUJILLO, M; RODRIGUEZ, A; GRACIA BARA, M; MATHEU, |
UBEIRA, F. 2000. Anisaquiosis y alergia. Un |
VALLS, A; PASCUAL, C; MARTÍN M. 2003. |
VAN THIEL, P.H.; KUIPERS, F.C.; ROSKAM, R.T. 1960. |
WHO. 1989. Report of WHO Consultation on Public Borne Diseases. WHO/CDS/VPH/90.86. |
Anexos
ANEXO 1. Ciclo biológico de los
anisákidos.

ANEXO 2. Tríptico de AESAN para la
prevención de anisakiasis.


ANEXO 3. Cartel de AESAN para la prevención de
anisakiasis.

Autor:
María de los Angeles Tort
Hernández
Escola de Prevenció i Seguretat
Integral
UAB, Bellaterra
Octubre de 2010.
 Página anterior Página anterior |   Volver al principio del trabajo Volver al principio del trabajo | Página siguiente  |