
Title: Reacciones químicas – significado
A + B ? C + D
reactivos
productos
H2 + Cl2 ? HCl
condiciones
catalizadores

Title: Reacciones químicas – significado
Equivalencia de masa y energía (Einstein, 1879-1955):
?E = ?m . c2
Ley de conservación de la energía:
“La energía total de un sistema cerrado se mantiene constante, no se crea ni se destruye sino que se transforma”
Ley de conservación de la masa (Lavoisier, 1743-1794):
“La masa total de un sistema cerrado se mantiene constante, independientemente de los cambios físicos o químicos que en él se produzcan”
Title: Reacciones químicas – significado
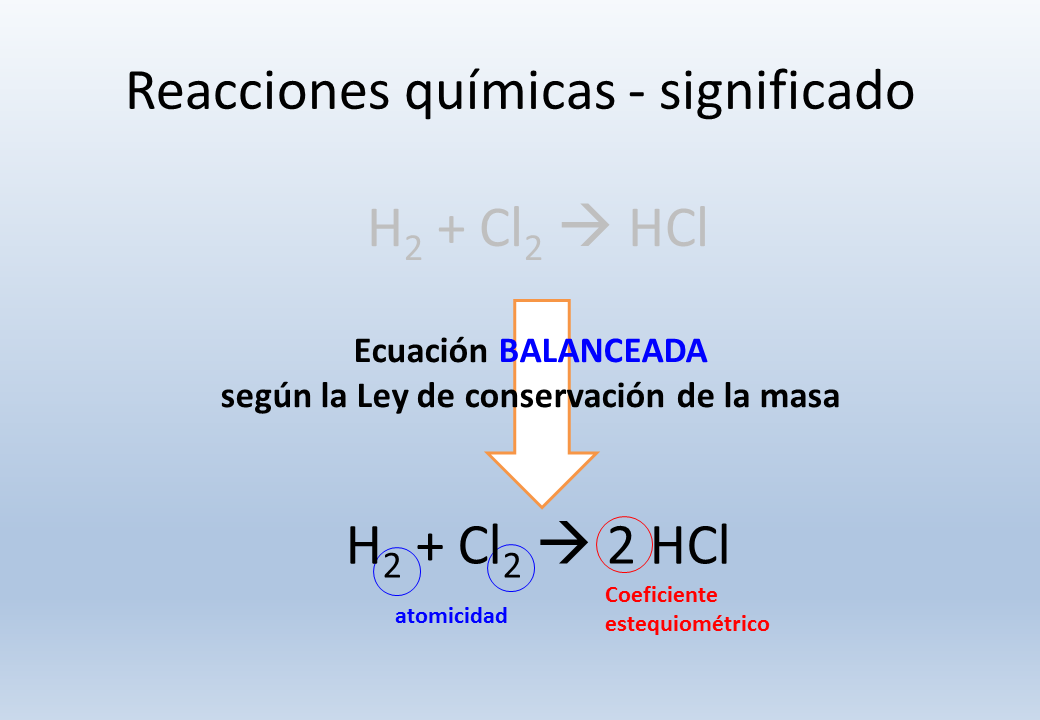
H2 + Cl2 ? HCl
Coeficiente estequiométrico
atomicidad
Ecuación BALANCEADAsegún la Ley de conservación de la masa
H2 + Cl2 ? 2 HCl

Title: Reacciones químicas – clasificación
Other Placeholder: Según la cantidad de reactivos y productos que intervienen…
Según haya o no variación en el número de oxidación…
Según haya liberación o absorción de energía…

Title: Reacciones químicas – clasificación
Other Placeholder: Según la cantidad de reactivos y productos que intervienen:
COMBINACIÓN, ADICIÓN, SÍNTESIS o POLIMERIZACIÓN.
DESPLAZAMIENTO o SUSTITUCIÓN:
Simple.
Doble.
DESCOMPOSICIÓN.

Title: Reacciones químicas – clasificación
Other Placeholder: COMBINACIÓN, ADICIÓN, SÍNTESIS o POLIMERIZACIÓN.
MgO + SO3 ? MgSO4
CaO + H2O ? Ca(OH)2
n CH2=CH2 ? -(CH2-CH2)-n
A + B ? AB

Title: Reacciones químicas – clasificación
Other Placeholder: DESPLAZAMIENTO o SUSTITUCIÓN:
Simple.
Doble.
CuSO4 + Fe ? FeSO4 + Cu
H2SO4 + 2 NaOH ? Na2SO4 + 2 H2O
AB + CD ? AC + BD
A + BC ? AB + C

Title: Reacciones químicas – clasificación
Other Placeholder: DESCOMPOSICIÓN.
CaCO3 ? CaO + CO2
2 HgO ? 2 Hg + O2
AB ? A + B

Title: Reacciones químicas – clasificación
Other Placeholder: Según haya o no variación en el número de oxidación:
METÁTESIS:
Precipitación.
Neutralización.
ÓXIDO-REDUCCIÓN o REDOX:
Desplazamiento de halógenos, metales o H.
Combustión.
Electroquímicas.

Title: Reacciones químicas – clasificación
Other Placeholder: Número de oxidación: …
La oxidación se define como la pérdida de electrones, cuando un elemento se oxida pierde electrones y por lo tanto aumenta su número de oxidación.
La reducción se define como la ganancia de electrones, cuando un elemento se reduce gana electrones y por lo tanto disminuye su número de oxidación.
Página siguiente  |