Dispersión de luz

Dispersión de luz Por qué el cielo es azul?
Cómo se ve el cielo de la luna? 1

Dispersión de luz John William Strutt Lord Rayleigh
2
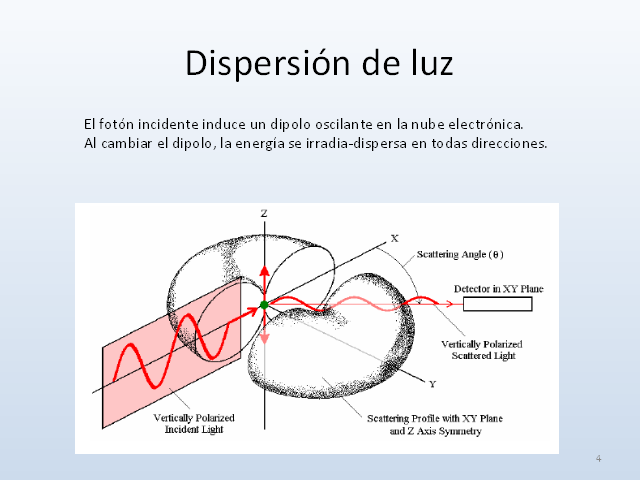
Dispersión de luz El fotón incidente induce un
dipolo oscilante en la nube electrónica. Al cambiar el
dipolo, la energía se irradia-dispersa en todas
direcciones. 3

Dispersión de luz por proteínas Intensidad de luz
dispersada es proporcional a la masa molecular y
concentración Sensible a la presencia de pequeñas
cantidades de agregados Polidispersity (homogeneidad) control de
calidad, cristalización de proteínas 4

Dispersión de luz por proteínas Se puede analizar
de diferentes maneras: Intensidad promedio (Estática)
(SLS, static light scattering) Fluctuaciones en la intensidad
(Dinámica) (DLS, dynamic light scattering) 5

Dispersión de luz estática Medida de masas
moleculares Intensidad promedio de dispersión es
función de la masa molecular y el 2do coeficiente virial K
= constante óptica MM = masa molecular A2 = 2do
coeficiente virial C = Concentración (g/L) Rq =
relación de Rayleigh (término que incluye la
intensidad) 6

Dispersión de luz estática Constante Factor de
forma, = 1 si r < 60 nm Relación de Rayleigh (para rm
< l/10) 7

Dispersión de luz estática La intensidad de luz
dispersada que produce una macromolécula es proporcional
al producto de la masa molecular promedio y la
concentración de la macromolécula (I a MM.C) Si no
hay dependencia entre la intensidad de dispersión y el
ángulo de medida, se puede determinar MM con medidas en un
solo ángulo Un gráfico de Debye permite la
determinación de: MM absoluta 2do coefciente virial (A2)
8

Dispersión de luz estática Gráficos de
Debye: Preparar un número de concentraciones de la
proteína en un buffer apropiado 9

Dispersión de luz estática Ecuación de
Rayleigh Una gráfica de KC/Rq vs C debería dar una
linea recta cuyo intercepto a cero concentración
será 1/MW y el gradiente A2 10

Dispersión de luz estática 11

Dispersión de luz estática 12

Dispersión de luz estática 2do coeficiente virial
Propiedad termodinámica que describe la fuerza de
interacción entre la molécula y el solvente Si A2
> 0, las moléculas tienden a permanecer en
solución (la proteína prefiere el buffer) Si A2 = 0
la fuerza de la interacción proteína-solvente es
equivalente a la fuerza de la interacción
proteína-proteína (el solvente se llama solvente
theta) Si A2 < 0, la proteína tiende a precipitar o
agregar 13

Dispersión de luz estática 14

Dispersión de luz estática 15 Masa molecular de
proteínas

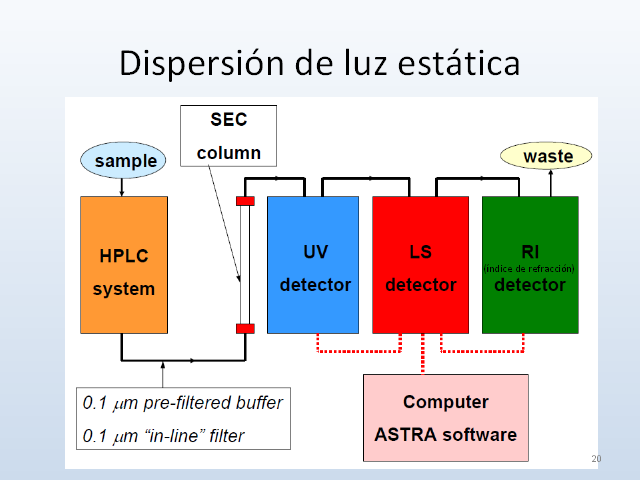
Dispersión de luz estática Medidas En batch/cubeta
En línea combinado con un paso de fraccionamiento,
principalmente Cromatografía de exclusión molecular
16

Dispersión de luz estática La masa molecular medida
en experimentos de dispersión son MM promediada por el
peso (fracción en g) Para un sistema simple de dos
componentes con proteína monomérica y agregados:
17

Dispersión de luz estática Para determinar MM
individuales: Fraccionar la muestra Combinar medidas de
dispersión con un paso de fraccionamiento ? SEC / MALS
18
Dispersión de luz estática 19 (índice de
refracción)

Dispersión de luz estática 20

Dispersión de luz estática 21

Dispersión de luz estática 22 (índice de
refracción)

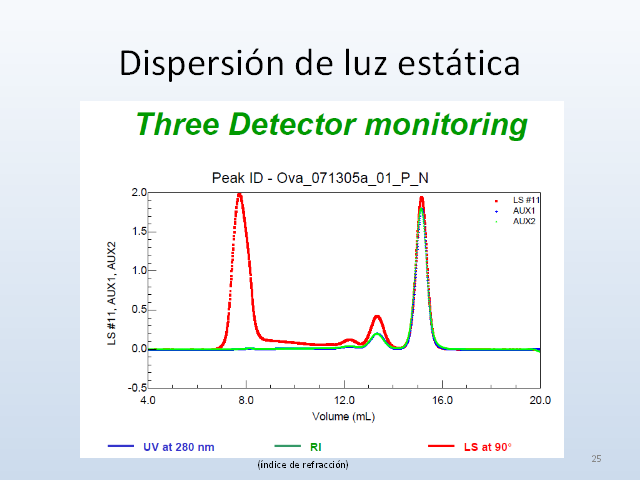
Dispersión de luz estática Señal de
dispersión Rq a MM C Debido a alta MM, los agregados
dispersan fuertemente Variación angular en la Intensidad
de luz dispersada se relaciona con el tamaño de la
molécula La luz dispersada por agregados muestra
dependencia angular, mientras que la luz dispersa por
monómeros y dímeros no. 23
Dispersión de luz estática 24 (índice de
refracción)

25

26

Dispersión de luz estática 27

Dispersión de luz estática 28

Dispersión de luz estática 29

Dispersión de luz estática Pros Determinacion de MM
rapida y exacta (promedio) de macromoleculas en solución
Combinando SEC-MALS se puede determinar MM con una precision
± 5% Dependencia angular de señal de LS detecta
agregados SEC-MALS permite detectar y cuantificar poblaciones de
proteinas según sus MM Puede determinar estado oligomerico
de polipeptidos modificados (prot-acidos nucleicos, glicosilados,
etc. 30 Contras Mide MM promedio, necesita separación para
distinguir estados oligoméricos Posible perdida de muestra
durante filtración y fraccionamiento

Dispersión de luz Dinámica 31

Dispersión de luz Dinámica 32 DLS Permite
determinar el tamaño de moléculas y
nanopartículas Mide las fluctuaciones en la intensidad de
dispersión con el tiempo para determinar el coeficiente de
difusión translacional (D), y luego el radio
hidrodinámico La velocidad de fluctuaciones depende del
tamaño de la partícula – molécula

Dispersión de luz Dinámica 33 Fluctuaciones son
resultado del movimiento browniano y puede correlacionarse con el
coeficiente de difusión y el tamaño

Dispersión de luz Dinámica La temperatura tiene que
ser estable y exactamente determinada (regular la viscosidad y
evitar la convección) Las partículas más
grandes se mueven más lentamente A mayor temperatura,
más rápido se mueven las moléculas La
velocidad del movimiento Browniano está definido por el
coeficiente de difusión translacional (D) 34

Dispersión de luz Dinámica Las fluctuaciones en la
intensidad no son al azar, sino consecuencia del confinamiento de
las partículas a sitios cercanos a la posición
inicial en tiempos muy cortos 35

Dispersión de luz Dinámica 36
Autocorrelación
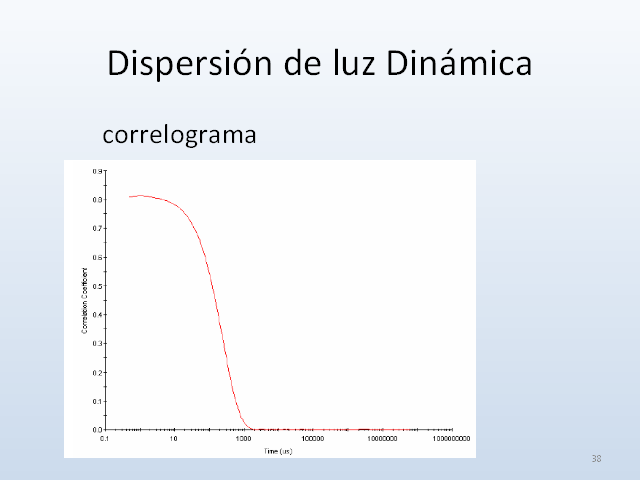
Dispersión de luz Dinámica correlograma 37

Dispersión de luz Dinámica 38

Dispersión de luz Dinámica 39

Dispersión de luz Dinámica 40
Dispersión de luz Dinámica 41

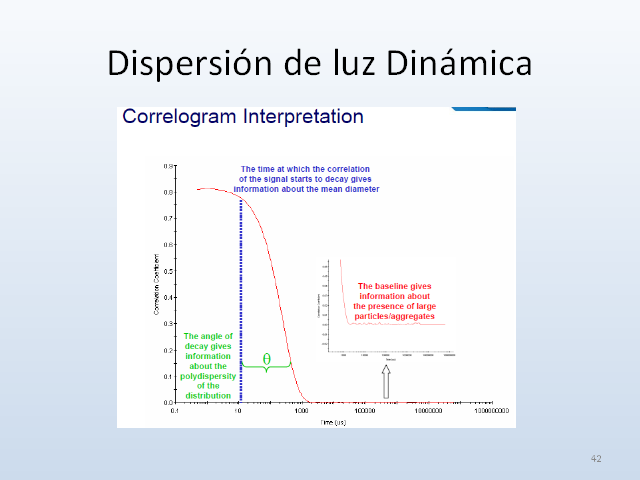
Dispersión de luz Dinámica 42

Dispersión de luz Dinámica 43
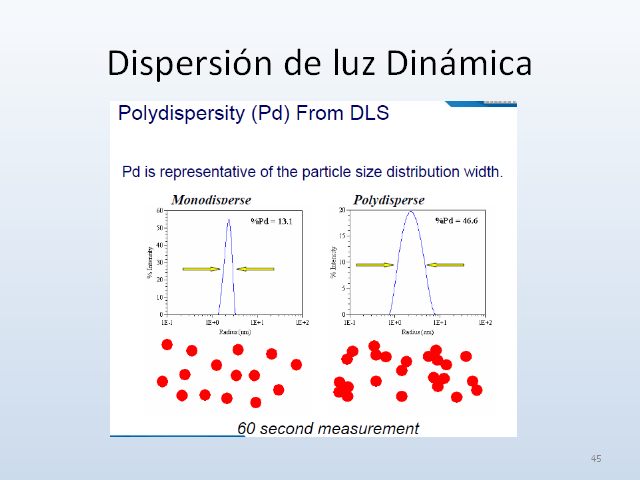
Dispersión de luz Dinámica 44
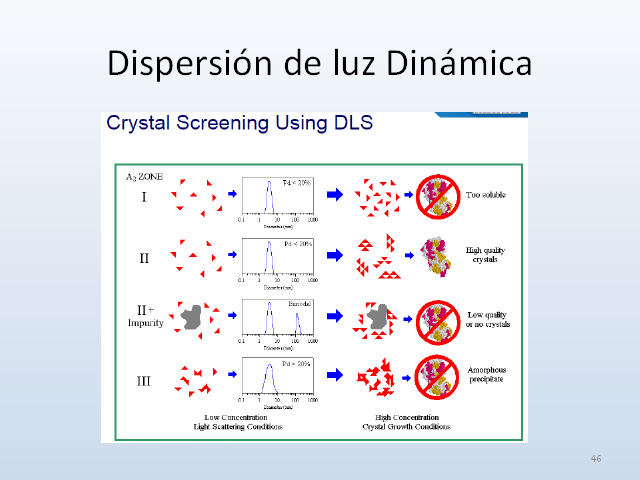
Dispersión de luz Dinámica 45
Dispersión de luz Dinámica 46

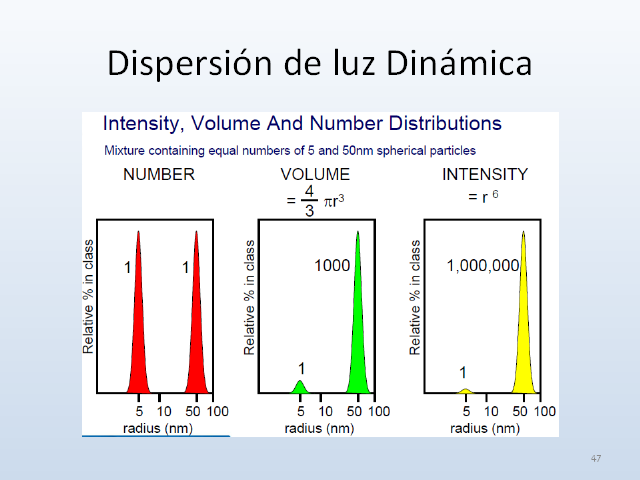
Dispersión de luz Dinámica 47

Dispersión de luz Dinámica Pros En cubeta, muy
rápida detección de agregados y evaluación
de la polidispersión de la muestra con un amplio rango
dinámico Adecuado para estudiar cinética de
agregación Detector disponible para placas, parara
screening Contras Mide radio hidrodinámico, es cual es
afectado por la forma de la partícula No puede distinguir
entre cambios de forma o estado de oligomerización
Necesita fraccionamiento para resolver oligómeros
presentes en una mezcla 48