
CONTENIDO 1.- Espontaneidad. Necesidad de una segunda ley. 2.-
Segundo Principio de la Termodinámica. Entropía.
3.- Cálculos de entropía. 4.- Entropías
absolutas. Tercer principio de la Termodinámica 5.-
Interpretación molecular de la entropía

¿Por qué unos procesos ocurren en un sentidoy no en
el contrario?

SEGUNDO PRINCIPIO Todo sistema aislado evoluciona en un sentido
hasta alcanzar el equilibrio 20ºC 25ºC ? El tiempo va
en una dirección (Gp:) . (Gp:) ? (Gp:) ?

ESPONTANEIDAD. NECESIDAD DE UNA SEGUNDA LEY. 1 Cambio
espontáneo: Aquél que tiende a ocurrir sinnecesidad
de ser impulsado por una influencia externa. ¿Se puede
explicar la direccionalidad del tiempo, con el primer principio
de la Termodinámica? No (Gp:) ? (Gp:) 25ºC (Gp:)
T=75ºC (Gp:) T=50ºC
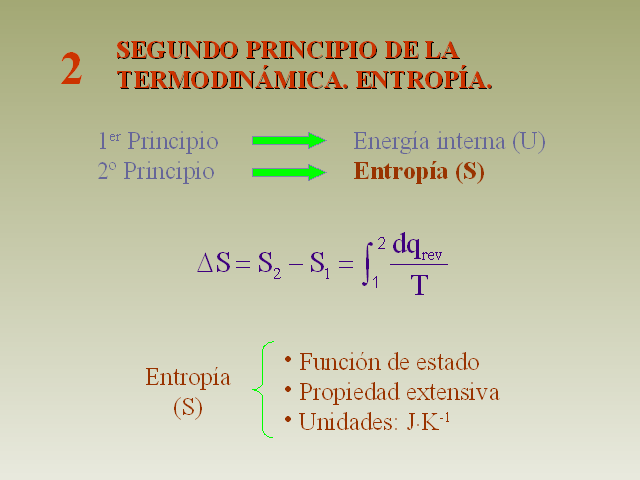
SEGUNDO PRINCIPIO DE LATERMODINÁMICA. ENTROPÍA. 2
(Gp:) 1er Principio Energía interna (U) 2º Principio
Entropía (S) (Gp:) Entropía (S) (Gp:)
Función de estado Propiedad extensiva Unidades:
J×K-1

Es imposible la transformación completa de calor en
trabajo en un proceso cíclico Primer Principio ES
IMPOSIBLE GANAR A LA NATURALEZA Segundo Principio ES IMPOSIBLE
INCLUSO EMPATAR (Gp:) Fuente de calor (Gp:) Máquina
Térmica (Gp:) Fuente Fría (Gp:) TC (Gp:) TC (Gp:)
QC (Gp:) QC (Gp:) W (Gp:) isotérmico (Gp:)
adiabático (Gp:) adiabático (Gp:) isotérmico
(Gp:) 4 (Gp:) 1 (Gp:) 3 (Gp:) 2 (Gp:) P (Gp:) V Q W

Cualquier proceso que ocurre espontáneamente produce un
aumento de entropía del universo Segundo Principio de la
Termodinámica Criterio de espontaneidad: DSuniv > 0
(Gp:) tiempo (Gp:) S (Gp:) univ (Gp:) proceso (Gp:)
equilibrio

En todo sistema en equilibrio, la entropía del universo
permanece constante. En todo proceso irreversible, la
entropía del universo aumenta. Segundo Principio de la
Termodinámica (Gp:) Sistema en equilibrio: DSuniv = DSsis
+ DSent = 0 Proceso irreversible: DSuniv = DSsis + DSent > 0
desigualdad de Claussius: DSuniv = 0 (Gp:) espontáneo
(Gp:) p. reversible

Caso particular: Sistema aislado (Gp:) Cualquier proceso deja a
los alrededores sin modificación alguna DSent = 0 Þ
DSuniv = DSsis (Gp:) Proceso reversible, sistema aislado: DSsis =
0 Proceso irreversible, sistema aislado: DSsis > 0 ¡Ojo!
Si no está aislado: Hay que tener en cuentala
variación de entropía del sistema y la de los
alrededores. En un proceso espontáneo aumenta la S del
universo.

La entropía puede considerarse como una medida de la
probabilidad (desorden) (Gp:) S (Gp:) Sólido (Gp:)
Líquido (Gp:) Gas (Gp:) S (Gp:) S Soluto +
Disolvente Disolución S

¿Cómo es que el agua a menos de 0ºC congela
espontáneamente?¿Acaso no disminuye la
entropía? DSuniv = DSsis + DSent > 0 (Gp:) < 0 (Gp:)
> 0

CÁLCULOS DE VARIACIÓN DE ENTROPÍA. 3 3.1.
Proceso Cíclico. Sistemas cerrados (Gp:) En un proceso
cíclico el estado final es el inicial, con independencia
de si es reversible o irreversible. 3.2. Proceso
Adiabático Reversible. (Gp:) En un proceso
adiabático reversible dqrev=0, luego ?S=0. En un
proceso adiabático irreversible dqrev=???
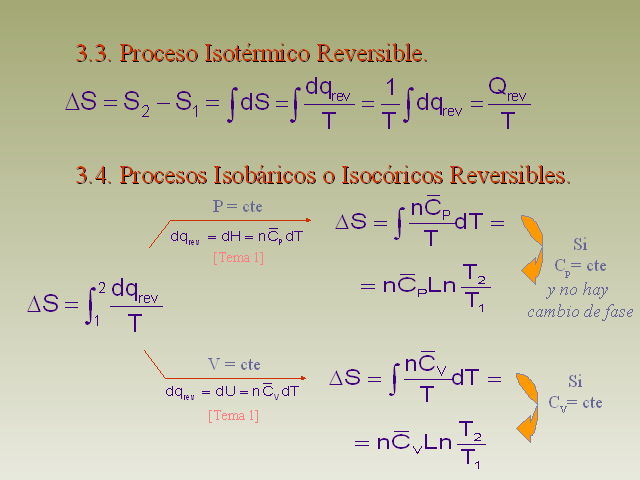
3.3. Proceso Isotérmico Reversible. 3.4. Procesos
Isobáricos o Isocóricos Reversibles. (Gp:) P = cte
(Gp:) [Tema 1] (Gp:) SiCp= cte y no hay cambio de fase (Gp:) V =
cte (Gp:) [Tema 1] (Gp:) SiCV= cte

3.5. Cambio de Fase, [(T, P) = constantes]. Evaporación
(líquido gas) ?Hvap >0 luego ?Svap >0
Sublimación (sólido gas) ?Hsub >0 luego ?Ssub
>0 Fusión (sólido líquido) (Gp:) > 0
(Gp:) > 0 > 0 Slíq > Ssol ; DSfus = Slíq-
Ssol > 0

3.6. Cambio de Estado (Reversible o Irreversible) de un Gas Ideal
(Gp:) dU=dqV=CVdT (Gp:) dU=dqrev+dwrev (Gp:) dwrev= – PdV
Función de estado Si CV es constante al ser la sustancia
es un Gas Ideal P/T = nR/V

ENTROPÍAS ABSOLUTAS.3er PRINCIPIO DE LA
TERMODINÁMICA. 4 (Gp:) Proporciona un origen de
entropías (Gp:) Podemos tabular entropías absolutas
La entropía de un elemento puro en su forma condensada
estable (sólido o líquido) es cero cuando la
temperatura tiende a cero y la presión es de 1 bar
“En cualquier proceso isotérmico que implique
sustancias puras, cada una en equilibrio interno, la
variación de entropía tiende a cero cuando la
temperatura tiende a cero”

El Tercer Principio permite conocer la entropía de
cualquier sustancia en el límite de 0 K (imaginando una
reacción química, a P=1bar, entre elementos a T=0K,
se obtendría cualquier compuesto a T=0K, y P=1bar y su S
sería 0 J/K). (Gp:) manteniendo P=1bar

INTERPRETACIÓN MOLECULARDE LA ENTROPÍA. 4 Un
sistema puede describirse de dos formas: *
Macroscópicamente (P, V, T) * Microscópicamente
(posición y velocidad de cada átomo) Con un estado
macroscópico hay muchos estados
microscópicoscompatibles. La entropía es una medida
del número de estados microscópicosasociados con un
estado macroscópico determinado. Estado
macroscópico: * Ordenado * Desordenado Estado
microscópico: * Orden exacto de los naipes

Un sistema desordenado es más probable que uno ordenado
porque tiene más estados microscópicos disponibles.
La entropía tiene una tendencia natural a aumentar dado
que corresponde al cambio de condiciones de baja probabilidad a
estados de probabilidad mayor. El Tercer Principio de la
Termodinámica implica que si fuera posible alcanzar el
“cero absoluto” de temperatura, la materia
estaría totalmente “ordenada”. En el
“cero absoluto de temperatura”, sólo hay una
posible disposición de las moléculas, Sº(0K)
=0 J/K. Al aumentar T, las moléculas, y los átomos
que las constituyen adquieren una cierta movilidad, con lo que
pueden adoptar varias orientaciones con la misma energía.
Son posibles por tanto más
“microestados”.

De forma muy aproximada y general, se puede decir que En igualdad
de condiciones (P,T), las S de los gases son mayores que las de
los líquidos y estas a su vez mayores que las de los
sólidos (recordad la idea de “mayor probabilidad,
mayor desorden) Sustancias con moléculas de tamaño
y estructura similar tienen entropías parecidas, a igual
(P,T) En reacciones químicas que impliquen sólo
gases, líquidos puros y sólidos puros, la ?Sº
del sistema dependerá en general de la variación
del número de moles de gas (si ngas aumenta ?Sº
>0, si ngas disminuye ?Sº<0) Entropía en
Química