
Heber Gabriel Pico Jiménez MD. Configuración
electrónica y la Nueva Tabla Periódica Electronic
configuration and the new periodic table Heber Gabriel Pico
Jiménez MD1 Resumen En este trabajo gracias a la nueva
regla del octeto se consigue la razón, del porqué
el Cinc tiene tanto parecido al Magnesio. Además se
demuestra que la ambivalencia habida en la configuración
electrónica del Lawrencio, obedece a la misma razón
que origina las anomalías electrónicas del cromo y
el cobre. Gracias a la nueva regla del octeto se demuestra que en
sí las configuraciones electrónicas, son realmente
una calcomanía resumida de la misma tabla
periódica, no basta con decir que son dos entidades
simplemente ligadas, no no señor, se trata de lo mismo, en
las configuraciones electrónicas los elementos tienen el
mismo ordenamiento que tienen los átomos en la tabla
periódica. Podemos decir que este trabajo unifica a la
tabla periódica, con la configuración
electrónica quien ya no debiera llamarse solo
electrónica, sino configuración de electrones y
huecos o configuración de partículas. Este trabajo
demuestra el porqué la línea inclinada,
limítrofe e irregular que separa a los metales de los no
metales, está ubicada en el bloque p de la tabla
periódica. Palabras claves: Tabla Periódica,
Configuración electrónica, Huecos. Abstract This
work thanks to the new rule of byte to obtain the reason, why the
zinc has both similar to magnesium. Also demon- strates that the
ambivalence in the electronic configuration of the Lawrencium is
due to the same reason that originates electronic anomalies of
chrome and copper. Thanks to the new rule of byte is shown that
itself the electronic configurations are actually a summary
sticker in the same periodic table, enough to say that they are
two simply-linked entities, not Lord, is not the same thing, in
the electronic configurations elements have the same order which
are the atoms in the periodic ta- ble. We can say that this work
unifies the periodic table; electronic configuration who already
should not call is only elec- tronics, but configuration of
electrons and holes or configuration of particles. This paper
shows why the sloping, bordering and irregular line that
separates the metals from the nonmetals is located in the block
of the periodic table p. Keywords: Periodic table, electronic
configuration, holes. © heberpico@hotmail.com todos los
derechos reservados1. 1. Introducción Precisamos que todo
el desarrollo de este artículo, estará siempre
sostenido en el principio de que químicamente los 1
electrones por lo general, estarán casi siempre apareados.
Bajo este principio se desarrollan los anteriores trabajos de
energía atómica Número cuántico
magnético del electrón, el trabajo de la
superconductividad, el artículo del acoplamien- to
espín-órbita del electrón, además el
anterior trabajo de Semiconductores y el de Células
fotoeléctricas publicado en

1 10 14 3 7 1 9 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 0 0 0 1 4 6
8 0 3 2 3 4 5 6 7 8 0 7 9 textoscientificos y Monografías.
También este artículo se basa en la nueva regla del
octeto. En la molécula de monóxido de carbono el
átomo de carbo- no se comporta como un nucleófilo
rico en electrones es decir como un carbanión. Este
trabajo está basado en el del estado fundamental del
átomo y los enlaces hipervalentes. Dentro los trabajos
anteriores también están el ácido
fluoroantimónico. Este artículo sustenta el origen
de la barrera interna de po- tencial que se origina en las
uniones PN, lo sustenta en base a la nueva regla del octeto que
utiliza al hueco como partí- cula subatómica y
extiende su explicación, a los dopajes del silicio con
elementos del grupo del oxígeno, el flúor, los
alcalinotérreos y los alcalinos. A este trabajo le es de
mucha utilidad los dopajes tipos N6P2 y la barrera interna de
potencial. 2. Desarrollo del Tema. La configuración
electrónica es importante porque determi- na las
propiedades de combinación química en los
átomos y por tanto su posición en la tabla
periódica. El número de partículas
(electrones+huecos) por cada nivel El último nivel de
energía de cualquier átomo con excep- ción
del hidrógeno y el helio, siempre tendrán dos
subnive- les y 8 partículas en el último nivel de
valencia. Bien, esa regla que acabamos de mencionar, se la
aplicamos no solamente a electrones sino que se la extendemos a
todas las partículas incluyendo a electrones y a huecos
del res- pectivo nivel como partículas. Ahora, el
número de partículas (electrones y huecos) que le
corresponden a cada subnivel de energía, ya sea s, p, d,
f, etc es de 2(2l+1), donde l es el subnivel de energía
que tomará valores de 0, 1, 2, 3, n-1 donde n es el primer
núme- ro cuántico. Pues igual, esos mismos
principios se los aplicamos a las partículas en general,
es decir que incluyan tanto a los elec- trones como a los huecos
del subnivel, considerando eso sí a los huecos como
partículas y aplicando a la nueva regla del octeto quien
dice que el número de partículas que debe tener un
subnivel l, es de 2(2l+1). Además los orbitales conservan
a las partículas es por pares cualquiera (electrones o
huecos) que sean, es decir que siempre en un orbital,
habrá un par de partículas, ya sean electrones o
huecos exclusivos o mixtos. Empezamos aplicando estas ambas
reglas a toda la tabla periódica de la siguiente manera
Nueva Tabla Periódica según la
Nueva Regla del Octeto de energía,
está regido por la siguiente fórmula: 2n2 donde 6 1
2 n es el primer número cuántico y además es
el número de subniveles de energía que tenga en ese
momento el respec- tivo nivel de energía. El número
de partículas (electro- nes+huecos) por niveles
energéticos depende del número total de niveles que
tenga el referido átomo porque siempre el último
nivel de energía, constará de solo dos subniveles
de energía que equivalen a 8 partículas
(electrones+huecos) y además, el subnivel d es una regla
de que se llene en el nivel inmediatamente anterior al
último nivel de valencia, mientras que el subnivel f, lo
hace en el nivel trans-anterior si se lo permite la formula 2n2,
el subnivel g en el nivel tras- trans-anterior también si
se lo permite la formula 2n2 por ejemplo, a los elementos que
tienen sus electrones de valen- cia en el quinto período
de la tabla periódica, al tercer nivel la formula 2n2 no
le permite tener más de 18 partículas por lo tanto
el subnivel f para ellos no tiene cabida mientras que en su
cuarto nivel le corresponde el llenado satisfactorio al subnivel
d. 2 3 4 5 6 7 8 9 0 1 1 1 1 1 1 1 1 1 2 3 4 5 6 7 8 2 2 2 2 2 2
2 2 2 2 3 3 3 3 3 3 3 0 1 2 3 4 5 6 7 8 9 0 1 2 3 4 5 6 3 3 4 4 4
4 4 4 4 4 4 4 5 5 5 5 5 8 9 0 1 2 3 4 5 6 7 8 9 0 1 2 3 4 5 5 5 5
5 6 6 6 6 6 6 6 6 6 6 7 7 7 7 7 7 7 7 7 7 8 8 8 8 8 8 8 5 6 7 8 9
0 1 2 3 4 5 6 7 8 9 0 1 2 3 4 5 6 7 8 9 0 1 2 3 4 5 6 1 1 1 8 8 8
9 9 9 9 9 9 9 9 9 9 0 0 0 0 0 0 0 1 1 1 1 1 1 1 1 7 8 9 0 1 2 3 4
5 6 7 8 9 1 2 5 1 1 2 5 1 Tabla periódica en que los
elementos están ordenados por su número
atómico donde por motivos de espacio las cifras de los
números atómicos quedan en forma vertical, centenas
sobre decenas y estas sobre las unidades del número
atómico. Hay un total de 32 grupos que numerados aumentan
de izquierda a derecha a medida que disminuye el número de
huecos en los grupos, hasta llegar a los halógenos que
tienen un solo hueco y en el extremo derecho se sitúan los
gases nobles que carecen de huecos. Figura No.1. En la tabla
periódica descrita en la figura No. 1, se puede ver como
las dos columnas de los alcalinos y alcalinotérreos se
corren hacia la derecha de la tabla, configurando nuevos
grupos.
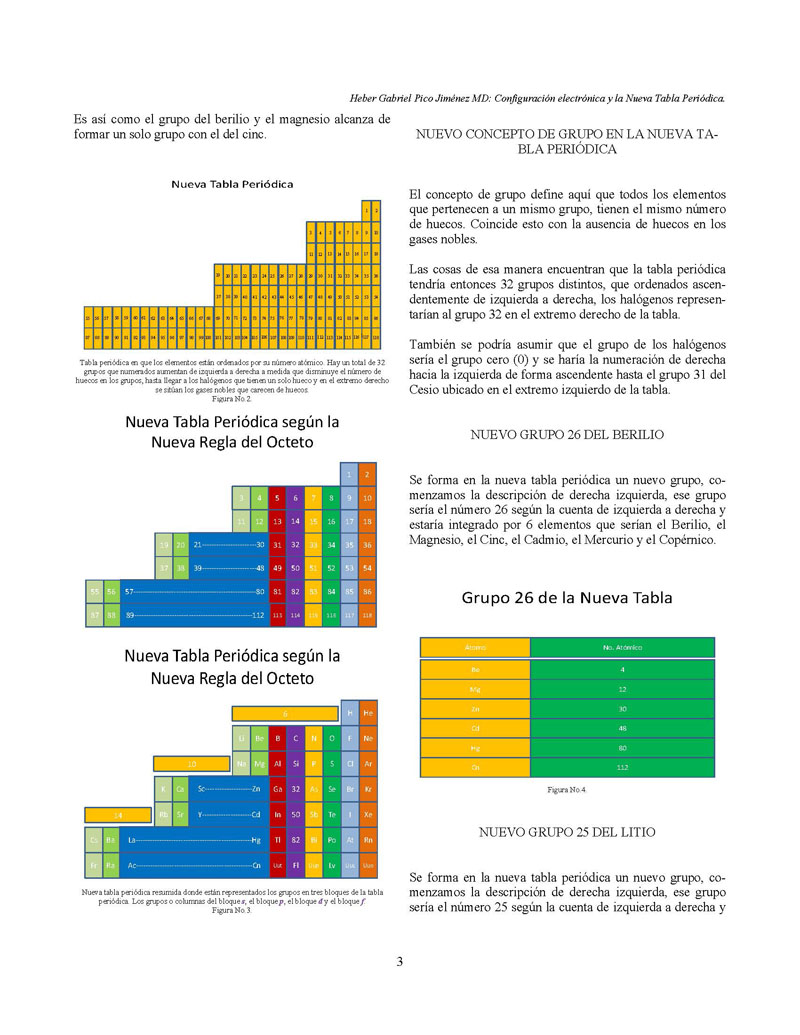
87 88 89 90 91 94 95 96 97 98 Es así como el grupo del
berilio y el magnesio alcanza de formar un solo grupo con el del
cinc. Nueva Tabla Periódica NUEVO CONCEPTO DE
GRUPO EN LA NUEVA TA- BLA PERIÓDICA El concepto de grupo
define aquí que todos los elementos 1 2 que pertenecen a
un mismo grupo, tienen el mismo número de huecos. Coincide
esto con la ausencia de huecos en los 3 4 5 6 7 8 9 10 gases
nobles. 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29
30 31 32 33 34 35 36 Las cosas de esa manera encuentran que la
tabla periódica tendría entonces 32 grupos
distintos, que ordenados ascen- 37 38 39 40 41 42 43 44 45 46 47
48 49 50 51 52 53 54 dentemente de izquierda a derecha, los
halógenos represen- 55 56 57 58 59 60 61 62 63 64 65 66 67
68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86
tarían al grupo 32 en el extremo derecho de la tabla. 92
93 99 100 101 102 103 104 105 106 107 108 109 110 111 112 113 114
115 116 1117 118 También se podría asumir que el
grupo de los halógenos Tabla periódica en que los
elementos están ordenados por su número
atómico. Hay un total de 32 grupos que numerados aumentan
de izquierda a derecha a medida que disminuye el número de
huecos en los grupos, hasta llegar a los halógenos que
tienen un solo hueco y en el extremo derecho se sitúan los
gases nobles que carecen de huecos. Figura No.2.
Nueva Tabla Periódica según la
Nueva Regla del Octeto sería el grupo cero
(0) y se haría la numeración de derecha hacia la
izquierda de forma ascendente hasta el grupo 31 del Cesio ubicado
en el extremo izquierdo de la tabla. NUEVO GRUPO 26 DEL BERILIO 1
2 Se forma en la nueva tabla periódica un nuevo grupo, co-
3 4 5 6 7 8 9 10 menzamos la descripción de derecha
izquierda, ese grupo sería el número 26
según la cuenta de izquierda a derecha y 11 12 13 14 15 16
17 18 estaría integrado por 6 elementos que serían
el Berilio, el 19 37 20 38 21———————–30
39———————–48 31 49 32 50 33 51 34 52 35 53 36 54
Magnesio, el Cinc, el Cadmio, el Mercurio y el Copérnico.
55 87 56 88
57—————————————————-80
89————————————————–112 81 113 82
114 83 115 84 116 85 117 86 118
Grupo 26 de la Nueva Tabla
Nueva Tabla Periódica según la
Nueva Regla del Octeto Átomo Be Mg
No. Atómico 4 12 6 H He Zn 30 Cd 48 Li Be B C N O F
Ne Hg 80 10 Na Mg Al Si P S Cl Ar Cn 112 K Ca
Sc——————–Zn Ga 32 As Se Br Kr Figura No.4. 14 Rb Sr
Y———————Cd In 50 Sb Te I Xe Cs Fr Ba Ra
La————————————————-Hg
Ac————————————————-Cn Tl Uut 82
Fl Bi Uup Po Lv At Uus Rn Uuo NUEVO GRUPO 25 DEL LITIO Se forma
en la nueva tabla periódica un nuevo grupo, co- Nueva
tabla periódica resumida donde están representados
los grupos en tres bloques de la tabla periódica. Los
grupos o columnas del bloque s, el bloque p, el bloque d y el
bloque f. Figura No.3. 3 menzamos la descripción de
derecha izquierda, ese grupo sería el número 25
según la cuenta de izquierda a derecha y

2 2 2 14 estaría integrado por 6 átomos que
serían el Litio, el Sodio, el Cobre, la Plata, el Oro y el
Roentgenio. Grupo 25 de la Nueva Tabla
Se forma en la nueva tabla periódica un nuevo grupo, co-
menzamos la descripción de derecha izquierda, ese grupo
sería el número 15 según la cuenta de
izquierda a derecha y estaría integrado por 4 elementos
que serían el Potasio, el Rubidio, el Tulio y el
Mendelevio. Grupo 15 de la Nueva Tabla
Átomo No. Atómico Átomo
No Atómico Li 3 Na Cu Ag Au Rg 11 29 47 79 111 K Rb
Tm Md 19 37 69 101 Figura No.5 Grupo 15 de la nueva tabla
periódica integrado por el potasio, rubidio, tulio y
mendelevio. Figura No.7 NUEVO GRUPO 16 DEL CALCIO
CONFIGURACIÓN ELECTRONICA Y LA NUEVA TA- BLA PERIODICA Se
forma en la nueva tabla periódica un nuevo grupo, co-
menzamos la descripción de derecha izquierda, ese grupo
sería el número 16 según la cuenta de
izquierda a derecha y estaría integrado por 4 elementos
que serían el Calcio, el La configuración
electrónica la sigue rigiendo el Principio de
Construcción en el Diagrama de Moeller. Estroncio, el
Iterbio y el Nobelio. La nueva regla del octeto no aplica estas
leyes solo para el número máximo de electrones, no,
no señor, ellas son apli-
Grupo 16 de la Nueva Tabla cadas para
los dos tipos de partículas, involucrando a los electrones
y a los huecos. Finalmente la configuración
electrónica queda como siem- Átomo Ca Sr Yb No
No. Atómico 20 38 70 102 pre ha sido tradicionalmente
aceptada de la siguiente mane- ra:
1s22s22p63s23p64s23d104p65s24d105p66s24f145d106p6-
7s25f146d107p68s25g186f147d108p69s26g187f148d109p6. Pero ordenada
por períodos o niveles energéticos, queda de la
siguiente forma, que es precisamente la misma estructura de la
nueva tabla periódica. Grupo 16 de la nueva tabla
periódica integrado por el calcio, el estroncio, el
Iterbio y el Nobelio. Figura No.6. NUEVO GRUPO 15 DEL POTASIO 4
1s2. 2s 2p6. 3s23p6. 4s 3d104p6. 5s24d105p6. 6s 4f 5d106p6.
7s25f146d107p6.

2 18 14 1 1 14 3 7 9 1 s 2 8s 5g 6f 7d108p6. 9s26g187f148d109p6.
Nueva Tabla Periódica según la
Nueva Regla del Octeto 6 1 2 Esta notación
anterior y siguiente representa exactamente a los períodos
de la nueva tabla periódica. 10 3 4 1 1 1 2 5 6 7 8 9 0 1
1 1 1 1 1 3 4 5 6 7 8 2 2 2 2 2 2 2 2 2 2 3 3 3 3 3 3 3 Hemos
ampliado la configuración electrónica hasta el
nove- no nivel de energía, con el fin de ilustrar
reglamentada la condición de que el último nivel de
energía, siempre estará 0 1 2 3 4 5 6 7 8 9 0 1 2 3
4 5 6 3 3 4 4 4 4 4 4 4 4 4 4 5 5 5 5 5 8 9 0 1 2 3 4 5 6 7 8 9 0
1 2 3 4 5 5 5 5 5 6 6 6 6 6 6 6 6 6 6 7 7 7 7 7 7 7 7 7 7 8 8 8 8
8 8 8 5 6 7 8 9 0 1 2 3 4 5 6 7 8 9 0 1 2 3 4 5 6 7 8 9 0 1 2 3 4
5 6 ocupado por 8 partículas que incluyen a electrones y a
hue- 8 8 8 9 9 9 9 9 9 9 9 9 9 7 8 9 0 1 2 3 4 5 6 7 8 9 1 1 0 0
1 0 1 1 1 0 2 2 1 0 3 1 0 4 1 0 5 5 1 0 6 1 1 0 7 1 0 8 1 1 0 9 1
1 0 1 1 1 1 1 1 2 1 1 3 1 1 4 1 1 5 1 1 6 1 1 7 1 1 8 cos en dos
subniveles, también es una regla de que el res- pectivo
orden de llenado de las partículas en los distintos
subniveles es el siguiente: El subnivel d siempre
aparecerá lleno de partículas en el nivel que es
anterior al último nivel de energía. Mientras que
el subnivel f sin embargo hará su aparición en el
nivel trans-anterior al último. Mientras que en ese orden
de aparición el subnivel g por su parte, solo
existirá lleno de partículas en el nivel
tras-trans-anterior. Decimos lleno de partículas porque
nos referimos a electro- nes o a huecos, aunque lentamente a
medida que se va in- crementando el número atómico,
los huecos van siendo reemplazados por los electrones de
izquierda a derecha pero generalmente de manera inversa es decir,
los electrones reemplazaran sino hay más subniveles
generalmente prime- ro a los huecos de menor energía que
serían los huecos g, después a los huecos f y
finalmente por ultimo a los huecos d que serían los huecos
con energía más cercana al último nivel.
Notación Espectral Nueva tabla periódica
según la nueva regla del octeto como imagen especular de
la distribución electrónica. Decimos imagen
especular para resaltar que generalmente el orden de reemplazar a
los huecos por los electrones es de acuerdo al estado de
excitación del respectivo átomo y es de f hacia d.
Figura No.9. ANOMALÍAS DE CONFIGURACIÓN
ELECTRÓNICA Hay casos que la literatura los describe como
excepciones en las configuraciones electrónicas pero, la
nueva regla del octeto demuestra que no son excepciones a la
norma sino puntos que confirman la regla porque en realidad son
esta- dos de menor energía en el mismo elemento por
ejemplo; a pesar de que por ahora se espera que el cromo 24
tuviera una configuración 1s2, 2s2, 2p6, 3s2, 3p6, 4s2,
3d4, 4p0 pero resulta, que en condiciones estándares el
cromo un electrón d tiene menos energía y
todavía, no ha tenido la energía suficiente para
saltar al cuarto nivel y por eso, presenta es una
configuración de 1s2, 2s2, 2p6, 3s2, 3p6, 4s1, 3d5, 4p0
que es su estado fundamental de menos energía en
determinadas condiciones de temperatura y presión. Nota
Aclaratoria: 4p0 quiere decir que en el cuarto nivel de
energía el subnivel p tiene cero electrones, porque se
quiere seguir en la notación espectral con la línea
que identifique 2 s 2 3 s 2 2 p 6 3 p 6 solamente a los
electrones, pero el subnivel p aunque no tiene electrones posee 6
huecos como partículas en el mis- mo cuarto nivel de
energía. 4 s 2 5 s 2 3 d 10 4 d 10 4 p 6 5 p 6 Igual pasa
con el cobre 29, la configuración electrónica 1s2,
2s2, 2p6, 3s2, 3p6, 4s1, 3d10, 4p0 es de menor energía que
la siguiente 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d9, 4p0. 6 s 2 7 s 2
4 f 5 f 14 14 5 d 10 6 d 10 6 p 6 7 p 6 Igual pasa con el
átomo de paladio 46, la configuración
electrónica 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s0,
4d10, 5p0 es de menor energía, que cualquier otra que
tenga elec- trones en el quinto nivel de energía. 8 s 2 5
g 18 6 f 14 7 d 10 8 p 6 Es la misma razón por la cual se
presenta la ambivalencia 9 s 2 6 g 18 7 f 14 8 d 10 9 p 6 en el
átomo de Lawrencio, donde por un lado se postula que es
[Rn]7s2,5f14,6d1 ,7p 0 , mientras la mecánica por otra
parte Distribución electrónica como una
calcomanía de la nueva tabla periódica. Vemos que
primero se reemplazan los huecos de subniveles menor
energía que serían los subniveles g en la tabla,
después seguirán los f y finalmente los d que es el
subnivel que tiene la cantidad de energía más
cercana al valor de la energía que tiene el último
nivel de energía. Figura No.8 5 propone una
configuración que es mucho más energética
como se puede ver [Rn]7s2,5f14,6d0,7p1, donde el electrón
d ha saltado del sexto al séptimo nivel de energía,
entonces

dica. ambas configuraciones son correctas pero dependen de las
condiciones de presión y temperatura que deben ser distin-
tas. El Lawrencio acaba con la premisa que tiene la acade- mia de
querer clasificar a un elemento como actínico o de
transición, no señor, desde aquí queremos
enviarle un men- saje a la IUPAC, donde le decimos que la
cuestión del orden de llenado de los bloques s, p, d, f, g
etc, es asunto que no le pertenecen a los grupos de la tabla, lo
gobiernan los perío- dos de la misma y que esa
clasificación de elementos de transición, no tiene
cabida en la nueva tabla periódica. Cuando se nos pregunte
por la distribución electrónica de un determinado
átomo, basta con saber cuántos electrones tiene
dicho elemento y con ello deducimos en que período de la
tabla periódica tiene ubicado su nivel más externo,
o de valencia, con ello determinamos cuantos huecos tiene y con
ello, definir el grupo que le pertenece en la tabla perió-
La cantidad de partículas que se encuentran en un nivel de
c) LA TERCERA GRAN CONCLUSIÓN es que los ele- mentos de un
mismo tercer período, tienen todos la misma
configuración particular extra nuclear por ejemplo, el
Sodio tiene la misma configuración de partículas
extra nucleares que el Argón donde es [Ne]3s2,3p6 esto
quiere decir que ambos tienen un total de 18 partículas
extra nucleares pero en el Sodio 11 de ellas son electrones y 7
son huecos mien- tras que en el Argón todas las 18
partículas extra nucleares son electrones. d) LA CUARTA
GRAN CONCLUSIÓN es que los elemen- tos de un mismo cuarto
período, tienen todos la misma configuración
particular extra nuclear por ejemplo, el Pota- sio tiene la misma
configuración de partículas extra nuclea- res que
el Kriptón donde es [Ar+3d10]4s2,4p6 esto quiere decir que
ambos tienen un total de 36 partículas extra nu- cleares
pero en el Potasio 19 de ellas son electrones y 17 son huecos
mientras que en el Kriptón todas las 36 partícu-
las extra nucleares son electrones. energía depende de la
cantidad de subniveles que tenga dicho nivel. e) LA QUINTA GRAN
CONCLUSIÓN es la nueva confi- Además también
depende de si es el nivel más externo del átomo o
nivel de valencia quien siempre tendrá 8 partículas
en dos subniveles. guración de partículas extra
nucleares del Kriptón que sería la siguiente
[Ar+3d10]4s2,4p6 esto quiere decir que el tercer nivel de los
elementos del 4º. Período de la tabla
periódica tiene 18 partículas y no es el mismo
tercer nivel del Argón mucho menos el del Kriptón
donde todos los huecos han sido reemplazados por electrones. 3-
Conclusiones: f) LA SEXTA GRAN CONCLUSIÓN es que los
elementos de un mismo quinto período, tienen todos la
misma configu- a) LA PRIMERA GRAN CONCLUSIÓN es que los
ele- mentos de un mismo período, tienen todos la misma
confi- guración de partículas extra nucleares por
ejemplo, el Hidrógeno tiene la misma configuración
de partículas extra nucleares que el Helio donde es 1s2,
esto quiere decir que ambos tienen un total de dos
partículas extra nucleares pero, en el Hidrógeno
una de ellas es un electrón mientras que en ración
particular extra nuclear por ejemplo, el Rubidio tiene la misma
configuración de partículas extra nucleares que el
Xenón donde es [Kr+4d10]5s2,5p6 esto quiere decir que
ambos tienen un total de 54 partículas extra nucleares
pero en el Rubidio 37 de ellas son electrones y 17 son huecos
mientras que en el Xenón todas las 54 partículas
extra nu- cleares son electrones. el Helio ambas
partículas extre nucleares son electrones. g) LA SEPTIMA
GRAN CONCLUSIÓN es que los ele- b) LA SEGUNDA GRAN
CONCLUSIÓN es que los ele- mentos de un mismo segundo
período, tienen todos la mis- ma configuración
particular extra nuclear por ejemplo, el Litio tiene la misma
configuración de partículas extra nu- cleares que
el Neón donde es [He]2s2,2p6, esto quiere decir que ambos
tienen un total de 10 partículas extra nucleares pero en
el Litio 3 de ellas son electrones y 7 son huecos mientras que en
el Neón todas las 10 partículas extra nu- cleares
son electrones. 6 mentos de un mismo sexto período, tienen
todos la misma configuración particular extra nuclear por
ejemplo, el Cesio tiene la misma configuración de
partículas extra nucleares que el Radón donde es
[Xe+4f14+5d10]6s2,6p6, esto quiere decir que ambos tienen un
total de 86 partículas extra nu- cleares pero en el Cesio
55 de ellas son electrones y 31 son huecos mientras que en el
Radón todas las 86 partículas extra nucleares son
electrones.

2 2 2 14 2 h) LA OCTAVA GRAN CONCLUSIÓN es que los ele-
mentos de un mismo séptimo período, tienen todos la
mis- ma configuración particular extra nuclear por
ejemplo, el Francio tiene la misma configuración de
partículas extra nucleares que tiene el elemento sintetico
del Ununoctio donde la configuración es
[Rn+5f14+6d10]7s2,7p6, esto quie- re decir que ambos tienen un
total de 118 partículas extra nucleares pero en el Francio
87 de ellas son electrones y 31 son huecos mientras que en el
Ununoctio todas las partícu- las exte nucleares son
electrones. i) LA NOVENA GRAN CONCLUSIÓN es la nueva orga-
nización que adoptaría la configuración de
partículas extra nucleares de cualquier átomo y que
incluye a electrones y a huecos, quien además
reemplazaría al diagrama de Moeller 4- Referencias 1s2. 2s
2p6. 3s23p6. 4s 3d104p6. 5s24d105p6. 6s 4f 5d106p6.
7s25f146d107p6. 8s 5g186f147d108p6. 9s26g187f148d109p6. con
ventajas porque incluiría a electrones y a huecos y
además, las notaciones no deben ser en diagonales sino
horizontales de izquierda a derecha y de arriba hacia abajo:
REFERENCIAS DEL ARTÍCULO. [1] Nueva tabla
periódica. Notación Espectral 1 s 2 [2] Nueva
tabla periódica. [3] Ciclo del Ozono [4] Ciclo del Ozono
[5] Barrera Interna de Potencial [6] Barrera Interna de Potencial
2 s 2 3 s 2 2 p 6 3 p 6 [7] Ácido Fluoroantimónico.
[8] Ácido Fluoroantimónico. [9] Dióxido de
cloro [10]Dióxido de cloro 4 s 2 5 s 2 3 d 10 4 d 10 4 p 6
5 p 6 [11]Pentafluoruro de Antimonio [12]Pentafluoruro de
Antimonio [13]Tetróxido de Osmio [14]Enlaces Hipervalentes
6 s 2 4 f 14 5 d 10 6 p 6 [15]Enlaces en moléculas
Hipervalentes [16]Nueva regla del octeto [17]Estado fundamental
del átomo 7 s 2 5 f 14 6 d 10 7 p 6 [18]Estado fundamental
del átomo [19]Barrera rotacional del etano. 8 s 2 9 s 2 5
g 18 6 g 18 6 f 7 f 14 14 7 d 10 8 d 10 8 p 6 9 p 6 [20]Enlaces
de uno y tres electrones. [21]Enlaces de uno y tres electrones.
[22]Origen de la barrera rotacional del etano [23]Monóxido
de Carbono [24]Nueva regla fisicoquímica del octeto
Distribución electrónica como una calcomanía
de la nueva tabla periódica. Vemos que primero se
reemplazan los huecos de subniveles menor energía que
serían los subniveles g en la tabla, después
seguirán los f y finalmente los d que es el subnivel que
tiene la cantidad de energía más cercana al valor
de la energía que tiene el último nivel de
energía. Figura No.8 j) UNA DECIMA Y ULTIMA GRAN
CONCLUSIÓN es la manera como se obtiene la anterior tabla
o figura No.8 que es precisamente de la misma
configuración electrónica que todo mundo ha usado
de manera tradicional desde hace varias décadas. 7
[25]Células fotoeléctricas Monografías.
[26]Células Fotoeléctricas textoscientificos.
[27]Semiconductores Monografías. [28]Semiconductores
textoscientificos. [29]Superconductividad.
[30]Superconductividad. [31]Alotropía.
[32]Alotropía del Carbono. [33]Alotropía del
Oxigeno. [34]Ozono. [35]Diborano [36]Semiconductores y
temperatura.

REFERENCIAS DE LA TEORÍA [1] Número cuántico
magnético. [2] Ángulo cuántico [3] Paul
Dirac y Nosotros [4] Numero cuántico Azimutal monografias
[5] Numero cuántico Azimutal textoscientificos [6]
Inflación Cuántica textos científicos. [7]
Números cuánticos textoscientíficos.com. [8]
Inflación Cuántica Monografías [9] Orbital
Atómico [10] Números Cuánticos. [11]
Átomo de Bohr. [12] Líneas de Balmer. [13]
Constante Rydberg. [14] Dilatación gravitacional del
tiempo. [15] Número Cuántico magnético. [16]
Numero Cuántico Azimutal. Copyright © Derechos
Reservados1. Heber Gabriel Pico Jiménez MD1. Médico
Cirujano 1985 de la Universidad de Cartagena Colombia.
Investigador independiente de problemas biofísicos
médicos propios de la memoria, el apren- dizaje y otros
entre ellos la enfermedad de Alzheimer. Estos trabajos, que lo
más probable es que estén desfasados por la
poderosa magia secreta que tiene la ignorancia y la ingenuidad,
sin embargo, como cualquier representante de la comunidad
académi- ca que soy, también han sido debidamente
presentados sobretodo este se presentó el 6 de Enero del
2014 en la “Academia Colom- biana de Ciencias Exactas,
Físicas y Naturales” ACCEFYN. 8