 Página anterior Página anterior |   Voltar ao início do trabalho Voltar ao início do trabalho | Página seguinte  |
Foram utilizados dois solos: Podzólico Vermelho-Amarelo (PV) textura arenosa, com pH CaCl2, 4,1; MO 15 g.dm-3; P 14 mg.kg-1 (resina); e os cátions trocáveis, em mmolc.dm-3; 6,7 de K+; 16 de Ca2+; 5 de Mg2+ e 38 de H++Al3+; Latossolo Roxo (LR) textura muito argilosa, com pH CaCl2 4,8; MO 31 g.dm-3; P 46 mg.kg-1 (resina); e os cátions trocáveis, em mmolc.dm-3; 2,8 de K+; 64 de Ca2+; 13 de Mg2+ e 58 de H++Al3+. As amostras coletadas a 0-20 cm de profundidade, foram compostas, destorroadas, secas ao ar e peneiradas a 2 mm.
A vinhaça marcada com 15N foi produzida bioquimicamente conforme Lara Cabezas (1991) e empregada na quantidade de 100 mgN.kg-1 de solo, equivalendo a 100 m3.ha-1. A vinhaça-15N apresentou a seguinte composição química: pH 3,50; C total 13,30 g.kg-1; P2O5 0,43 g.kg-1; K2O 1,80 g.kg-1; cálcio 0,20 g.kg-1; magnésio 0,21 g.kg-1 e relação C/N 29,5. O fracionamento do N da vinhaça realizado conforme Lara Cabezas (1991), mostrou os seguintes valores: N solúvel 0,14 kg.m-3 (8,53 átomos % de abundância de 15N); N insolúvel 0,33 kg.m-3 (1,55 átomos % de abundância de 15N) e N total 0,47 kg.m-3 (3,629 átomos % de abundância de 15N).
Uréia de composição natural (uréia reagente p.a. Merck) foi utilizada na quantidade de 220 mgN.kg-1 solo (dose equivalente a 100 kg.ha-1).
Foi utilizada palha de cana-de-açúcar (folha + bainha) não marcada com 15N (seca e moída, contendo 510 mg.kg-1 de N-NH4+, 365 mg.kg-1 de N-NO3- e 3,1 g.kg1 de N-total), adicionada aos solos na quantidade de 22 g.kg-1 , equivalendo a 10 t.ha-1.
Os tratamentos constaram da aplicação aos solos PV e LR de vinhaça isoladamente (V*), de vinhaça e uréia (V*+U), de vinhaça e palha (V*+P), e de vinhaça mais uréia e palha (V*+U+P).
Amostras de 50 g de TFSA, foram mantidas em copos de plástico (capacidade de 100 ml), em condições de laboratório (25 ± 5ºC) em fração pré-determinada (± 80%) da capacidade de retenção de água do solo (PV 12 ml.50 g-1 solo; LR 19,5 ml.50 g-1 solo). Conforme os tratamentos, foram adicionadas a vinhaça (11,0 cm3, distribuída uniformemente sobre a superfície do solo), a uréia (1,0 cm3, na forma de solução com 11mg N.cm-3, distribuído também superficialmente) e a palha (1,1 g, previamente misturada em cada solo), acrescentando-se água para complementar a umidade pretendida. As doses equivalentes de vinhaça (m3.ha-1), N-uréia (kg.ha-1) e de palha (t.ha-1) foram calculadas considerando-se a profundidade de 4,5 cm de solo das parcelas (equivalente a 455.000 kg.ha-1 de solo).
As amostras, assim preparadas, foram incubadas por 7, 14, 21, 28 e 35 dias. Em cada período de incubação, seis repetições de cada tratamento foram recolhidas, sendo três destinadas às determinações de N-total e outras três às determinações dos teores de N-mineral: N-NH4+; N (NO3- +NO2-).
Durante o período de incubação foram feitos controles diários das perdas de água por evaporação (determinação dos níveis de umidade do solo), refazendo-se o peso inicial das parcelas experimentais, pela adição de água desionizada, quando necessário.
Determinações diárias do índice de acidez [pH em CaCl2 0,01M (1:2,5)], nas amostras dos solos PV e LR, foram realizadas em todos os trata-mentos, em parcelas separadas daquelas com 15N.
A determinação do N total nas amostras, seguiu a metodologia de Bremner & Mulvaney (1982). Os extratos destilados, após determinação do N total por titulometria, foram concentrados e pre-parados para determinação da abundância de 15N por espectrometria de massas (Trivelin et al., 1973).
As amostras de cada tratamento sofreram extração com KCl 2M (3:1), segundo recomendação de Buresh et al. (1982), procedendo-se a destilação dos extratos, conforme Keeney & Nelson (1982), para determinação das frações N-NH4+ e N-(NO3- + NO2-). Os extratos contendo as frações de N-amoniacal e N-nítrico foram concentrados para a determinação de abundância de 15N por espectrometria de massas (Trivelin et al., 1973).
Nos cálculos do nitrogênio no solo derivado da vinhaça (NsdV, em % e mg.kg-1), para o N-total e para o N-mineral (N-NH4+ e N-NO3- + N-NO2-), foram utilizadas as seguintes equações:
NsdV (%) = [(a - c)/(b - c)] . 100 (1)
NsdV (mg por parcela) = [NsdV (%) / 100] . NT (2)
onde: a e b representam, respectivamente, as abundâncias de 15N (átomo %), na amostra após o período experimental, e na vinhaça adicionada ao solo no início do experimento (3,629 átomos % de 15N); c é a abundância natural de 15N (0,366 átomos %) e NT é o nitrogênio total da amostra após o período experimental, em mg por parcela.
A parte do N total no solo derivado da vinhaça foi representada por NtsdV; as referentes ao N-NH4+ e ao N-NO3- no solo derivado da vinhaça, foram representadas, respectivamente, por NH4+sdV e NO3-sdV.
Os resultados de N-total das amostras, em cada período de incubação, permitiram determinar as perdas gasosas totais de nitrogênio da vinhaça (NvtdV, mg.parcela-1), pelo método indireto de balanço-15N, segundo a expressão:
NvtdV = NaV - NtsdV (3)
onde: Na V representou a quantidade de N da vinhaça-15N aplicada ao solo no início do experimento (tempo=0) e NtsdV o nitrogênio total no solo derivado da vinhaça-15N, após o período de incubação (tempo = t).
Adotou-se o delineamento experimental inteiramente casualizado. Os resultados foram submetidos à análise de variância, sendo comparadas as médias pelo teste de Tukey ao nível de significância de 5%. Foi procedida a análise de regressão dos valores de NH4+sdV, NO3-sdV e de NvtdV de cada tratamento versus tempo para definir as relações e suas correspondentes equações, sendo os níveis de significância avaliados pelo teste F ao nível de 5% de probabilidade.
N-NH4+ no solo derivado da vinhaça aplicada isoladamente e combinada com uréia e/ou com palha de cana-de-açúcar: De modo geral, foram baixas as quantidades do N-NH4+ derivado da vinhaça nos dois solos, em diferentes tempos de incubação. As maiores quantidades de N-NH4+ proveniente da vinhaça foram encontradas no tratamento V*+U com valor médio de 20,5 mg.kg-1 no PV e 16,4 mg.kg-1 no LR (Figuras 1a e 2a). A análise de variância das quantidades de N-NH4+sdV, para níveis eqüidistantes de tempo, mostrou-se significativa, ao nível de 5%. Verificou-se, que foram significativas, no tratamento V*+U, a regressão linear para o solo PV (Y = 30,13 - 0,42X, r = 0,82) e a quadrática para o solo LR (Y = 4,01 + 1,49X - 0,03X2, r = 0,93).
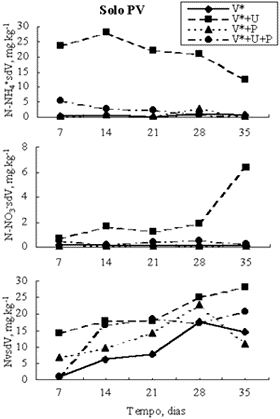
Figura 1.
N-NH4+, N-NO3- e N volatilizado proveniente da vinhaça no solo PV em função do tempo.
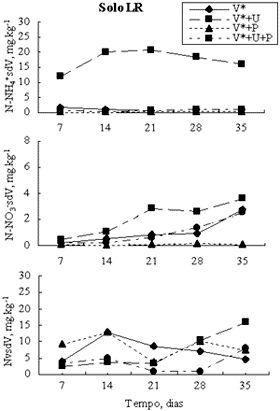
Figura 2.
N-NH4+, N-NO3- e N volatilizado proveniente da vinhaça no solo LR em função do tempo.
Os resultados sugerem que a uréia intensifica o processo de mineralização do N-vinhaça devido a uma maior disponibilidade de N-NH4+ para microbiota do solo. A diferença entre as médias dos solos PV e LR sugere que o N-NH4+ derivado da vinhaça foi influenciado pela natureza do solo, refletindo diferenças em características e propriedades, como textura, capacidade de retenção de água, aeração, entre outras, que provavelmente afetam a atividade dos microrganismos responsáveis pela mineralização do N-vinhaça.
Os tratamentos V*, V*+P e V*+U+P não mostraram diferenças entre si. Nesses tratamentos, as baixas quantidades do N-NH4+ derivado da vinhaça presente nos dois solos em diferentes tempos de incubação, podem ser atribuídas à imobilização líquida do N da vinhaça, pela microbiota, em resposta a adição da vinhaça e da palha, que apresentou elevada relação C/N. Em condições de campo, Vietes & Brinholi (1990) observaram acréscimos de N-NH4+ no período de 98 a 220 dias após a aplicação da vinhaça, até a profundidade de 20 cm. Nesse estudo, foi sugerida a amonificação do N-orgânico nativo do solo e/ou do N-orgânico da vinhaça, dada a alta proporção de N-solúvel prontamente mineralizável do resíduo. Sugere-se, portanto, um estudo em campo e mais prolongado.
N-NO3- no solo derivado da vinhaça aplicada isoladamente e combinada com uréia e/ou com palha de cana-de-açúcar: As quantidades de N-NO3-sdV dos tratamentos em função do tempo, oscilaram entre 6,4 a 0,02 mg kg-1 no solo PV e, 3,6 a 0,03 mg kg-1 no solo LR. O tratamento V*+U foi o que mostrou as maiores quantidades de N-NO3sdV (valor médio de 2,5mg.kg-1 no solo PV e de 2,2 mg.kg-1 no solo LR), com tendência de aumento ao longo do tempo para ambos os solos (Figuras 1b e 2b). Verificou-se, ainda, que foram significativas, ao nível de 5%, as regressões tratamento versus tempo, no tratamento V*+U para o solo PV (Y=3,19 - 0,126X, r= 0,80) e para o LR (Y= -0,22 + 0,11X, r= 0,95), e nos tratamentos V* (Y= -0,59 + 0,08X, r= 0,88) e V*+U+P (-0,68 + 0,08X, r= 0,93), para este último.
Estes resultados podem ser devido às alterações físico-químicas e na atividade da microbiota provocadas pela adição da vinhaça ao solo, principalmente na relação C/N, que induzem, num primeiro momento, a imobilização de N devido ao incremento na atividade da microbiota do solo e, num segundo momento, uma transformação a N-NO3-, lenta e gradual, até os vinte e oito dias, mais acentuadamente aos 35 dias. No tratamento V*+U a presença da uréia ampliou a nitrificação provavelmente devido à redução na relação C/N.
Os demais tratamentos mantiveram- se na mesma faixa no solo PV, no entanto, no LR, para os tratamentos V* e V*+P+U, o N-NO3- cresceu ao longo do tempo, sendo provavelmente reflexo da natureza do solo argiloso; neste, grande parte do amônio produzido foi nitrificada e parte pode ter sido perdida por volatilização, mas em intensidades menores que no solo PV. Amaral Sobrinho et al. (1983) verificaram perda de 18% do N-NO3- sob a forma volátil e um desaparecimento de 27% do N mineral devido ao processo de imobilização após a incubação de solo com vinhaça. Os autores sugerem que esse fenômeno seja devido à desnitrificação, dada a expressão de pulsos de N-NO2- e de N2O encontrados. A presença de material energético no solo, fornecido pela vinhaça, demandaria O2 para atender as necessidades metabólicas microbianas e, portanto, o N-NO3- poderia vir a ser reduzido em condições anóxicas.
Perdas de N da vinhaça em aplicação simples e em conjunto com uréia e/ou palha: As perdas do N da vinhaça determinadas pelo método indireto de balanço de 15N, representam, pelas condições experimentais impostas, perdas gasosas totais de nitrogênio da vinhaça. Elas serão referidas, de forma generalizada, como perdas por volatilização, não sendo distinguidas, portanto, quanto aos possíveis processos-causas, em particular nitrificação-desnitrificação e/ou volatilização de amônia. Estas perdas, nos solos PV e LR, não se mostraram significativamente diferentes entre os distintos tratamentos avaliados (Figuras 1c e 2c), embora, desde o inicio, o tratamento V*+U tenha apresentado valores mais elevados no PV que no LR, os quais, aos 35 dias de incubação, corresponderam a 28,27 mg.kg-1 e 16,00 mg.kg-1, respectivamente. No geral, as perdas do N da vinhaça foram crescentes com o decorrer do tempo e mais elevadas (14 %), em todos os tratamentos, no solo PV. No solo LR a perda média foi de 5%, com valores bem similares entre os tratamentos. Ademais, a análise de variância das quantidades do N volatilizado da vinhaça, para níveis eqüidistantes de tempo, detectou efeito significativo, ao nível de 5%, sendo a regressão linear significativa nos tratamentos V* (Y= -2,05 + 0,55X, r= 0,92) e V*+U+P (Y= 2.88 + 0,57X, r= 0,80) para o solo PV, e no tratamento V*+U (Y= -095 =0,43X, r= 0,91) para o solo LR.
Vale ressaltar ainda, que, no presente trabalho, foram observadas variações no índice de acidez do solo -pH (dados não apresentados) da ordem de 1,7 unidades, no solo PV, superiores às encontradas no solo LR. No início da incubação o pH foi de 3,9, oscilou durante o resto do período avaliado em torno de 5,6 e se manteve neste nível até 35 dias, enquanto a testemunha se estabeleceu em pH 4,5. Para o solo LR, o pH inicialmente observado foi de 4,9, atingiu valores de 6,6 no decorrer da incubação e se estabeleceu em 5,6 aos 35 dias; o pH da testemunha manteve-se em torno de 5,4 durante todo o período experimental. No solo PV, o pH manteve-se mais alto que o da testemunha, no final do experimento, enquanto no solo LR o pH final aproximou-se do da testemunha. Os efeitos da aplicação da vinhaça sobre o pH do solo são bem conhecidos, sendo, o comportamento observado, decorrente da oxidação da matéria orgânica (elevando o pH do solo), provocada pela população microbiana, que, atacando a matéria orgânica e decompondo-a parcialmente, diminui a acidez do solo. Essas inferências, no geral, concordam com observações semelhantes de outros autores (Almeida, 1953; Ferreira, 1980; Lima, 1980; Santos, et al., 1981; Rodella et al., 1983 e Mattiazzo & Glória, 1985).
De modo geral, os resultados obtidos refletem diferenças em características e propriedades dos solos PV e LR, indicando perdas mais elevadas no primeiro (textura arenosa), em relação ao segundo (textura argilosa), concordando com Ferreira (1980), que evidenciou comportamentos diferentes dependendo da textura do solo, e com outros autores (Chao & Kroontje, 1964; Gasser, 1964; Anjos & Tedesco, 1976; Buresh, 1987; Lara Cabezas, 1991), segundo os quais, em solo de textura arenosa e baixa CTC, a volatilização do N é mais efetiva. Além do mais, os resultados traduzem, ao lado dessas diferenças em características e propriedades, a influência dos efeitos da aplicação da vinhaça (dentre eles, a melhoria das propriedades físicas e químicas do solo, o aumento do poder de retenção de água, a elevação do pH do solo, como sugere Almeida, 1952), como possível ação associada, adicional ou promovedora, das variações nas perdas por volatilização observadas, durante o período avaliado, evidenciando aumentos das taxas de volatilização do nitrogênio em resposta à adição da vinhaça, aos solos estudados. Os resultados, no geral, assemelham-se aos obtidos por Lara Cabezas et al. (1994). Conforme Lara Cabezas (1991), a vinhaça contribui para elevação da taxa de volatilização do N, em decorrência da melhoria nas condições químicas do solo aliada à oferta de material orgânico com compostos voláteis de fácil decomposição, favorecendo a hidrólise da uréia pela maior retenção de água no solo. Em estudo sobre o efeito de resíduos orgânicos adicionados a solo tratado com uréia, Sengik & Kiehl (1995) encontraram que a vinhaça aumentou em 105% as perdas médias de amônia, quando comparada ao solo testemunha.
- As concentrações de N-NH4+ e N-NO3- proveniente da mineralização da vinhaça foram influenciadas pelo tipo de solo;
- A adição da uréia promoveu uma maior disponibili-dade de N-NH4+ e N-NO3- proveniente da vinhaça;
- Em presença de palha de cana-de-açúcar as concentrações nos solos de N-NH4+ e N-NO3- provenientes da vinhaça mostraram-se muito baixas, independentemente do tipo de solo;
- A adição conjunta de uréia e vinhaça em presença de palha não alterou as concentrações nos solos de N-NH4+ proveniente da vinhaça, e as concentrações de N-NO3- aumentaram apenas no solo LR;
- As perdas por volatilização de N vinhaça foram, em geral, crescentes, para todos os tratamentos no solo PV e mais elevadas (14 %) que no solo LR (5%); neste, foram praticamente constantes.
ALMEIDA, F.P. Interferência dos fungos na adubação do solo pela vinhaça. Piracicaba: ESALQ, Instituto Zimotécnico, 1953. 11p.
ALMEIDA, J.R. de O problema da vinhaça em São Paulo. Piracicaba: ESALQ, Instituto Zimotécnico, 1952. 9p. (Boletim, 3)
AMARAL SOBRINHO, N.M.B.; VELLOSO, A.C.X.; LEAL, J.R.; ROSIELLO, R.O.P. Desnitrificação e imobilização de nitrogênio em solo tratado com vinhaça. Revista Brasileira de Ciência do Solo, v.7, p.263-268, 1983.
ANJOS, J.T.; TEDESCO, M.J. Volatilização de amônia proveniente de dois fertilizantes aplicados em solos cultivados. Científica, v.4, n.1, p.49-55, 1976.
BREMNER, J.M; MALVANEY, C.S. Nitrogen-Total. In: PAGE, A.L.; MILLER, R.H.; KEENEY, D.R. (Ed). Methods of soil analysis. 2.ed. Madison: ASA, 1982. cap.31, p.595-624. (Agronomy, 9).
BURESH, R.J. Ammonia volatilization from point-placed urea in upland, sandy soils. Fertilizer Research, v.12, p.263-268, 1987.
BURESH, R.J.; AUSTIN, E.R.; CRASWELL, E.T. Analytical methods in 15N research. Fertilizer Research, v.3, p.37-62, 1982.
CAMARGO, R. O desenvolvimento da flora microbiana nos solos tratados com vinhaça. Piracicaba: ESALQ, Instituto Zimotécnico, 1954. 44p. (Boletim, 9)
CHAO, T.T.; KROONTJE, W. Relationships between ammonia volatilization, ammonia concentration and water evaporation. Soil Science Society of America Proceedings, v.28, p.393-395, 1964.
FERREIRA, W.A. Efeito da vinhaça em solos de diferentes texturas. Piracicaba, 1980. 67p. Dissertação (Mestrado) - Escola Superior de Agricultura "Luiz de Queiroz", Universidade de São Paulo.
GASSER, J.K.R. Some factors affecting losses ammonia from urea and ammonium sulfate apllied to soil. Journal of Soil Science, v.15, p.258-272, 1964.
KEENEY, D.R. ; NELSON, D.W. Nitrogen: inorganic forms. In: PAGE, A.L.; MILLER, R.H.; KEENEY, D.R. (Ed.). Methods of soil analysis. 2.ed. Madison: ASA, 1982. cap.33, p.643-689. (Agronomy, 9)
LARA CABEZAS, W.A.R. Marcação de vinhaça com 15N e avaliação de perdas gasosas de nitrogênio da vinhaça-15N e uréia-15N em solos cultivados com cana-de-açúcar (Saccharum spp). Piracicaba, 1991. 85p. Tese (Doutorado) - Escola Superior de Agricultura "Luiz de Queiroz", Universidade de São Paulo.
LARA CABEZAS, W.A.R.; TRIVELIN, P.C.O.; SCHIAVINATO JUNIOR, P.; BOARETTO, A.E. Perdas gasosas de nitrogênio de vinhaça e uréia em solos cultivados com cana-de-açucar. Revista Brasileira de Ciência do Solo, v.18, p.463-469, 1994.
LIMA, I.T. Efeitos da aplicação de vinhaça sobre a microflora do solo. Seropédica, 1980. 100p. Dissertação (Mestrado) - Universidade Federal do Rio de Janeiro.
MATTIAZZO, M.E.; GLORIA, N.A. Efeito da vinhaça na acidez do solo. STAB-Açúcar, Álcool e Subprodutos, v.4, n.2, p.35-40, 1985.
RODELLA, A.A.; ZAMBELLO, E.; FRANCISCO JUNIOR, J. O. Effects of vinasse added to soil on pH and exchangeable aluminum content. In: CONGRESS OF INTERNATIONAL SOCIETY OF SUGAR CANE TECHNOLOGISTS, 18., La Habana, 1983. Proceedings. La Habana: ISSCT, 1983. p.189-214.
SANTOS, G.A.; ROSSIELO, R.O.P.; FERNANDES, M. S.; O'GRADY, P.C. Efeitos da vinhaça sobre o pH do solo, a germinação e acúmulo de potássio em milho. Pesquisa Agropecuária Brasileira, v.16, p.489-493, 1981.
SENGIK, E.; KIEHL, J.C. Efeito de resíduos orgânicos e do fosfato monocálcico na volatilização de amônia em terra tratada com uréia. Revista Brasileira de Ciência do Solo, v.19, p.321-326, 1995.
TRIVELIN, P.C.O. ; SALATI, E. ; MATSUI, E. Preparo de amostras para análise de 15N por espectrometria de massas. Piracicaba: CENA, 1973. 41p. (Boletim Técnico, 2)
VIETES, R. L.; BRINHOLI, O. Efeito da aplicação de vinhaça na fração amônio do solo nas profundidades 20 cm. e 40 cm. Energia na Agricultura, v.5, n.4, p.11-26, 1990.
Vilma Maria Silva1; Paulo Cesar Ocheuze Trivelin2,5,*; Waldeciro Colaço1; Fernando Antonio Franco da Encarnação3; Waldo Alejandro Ruben Lara Cabezas4
pcotrive[arroba]cena.usp.br
1Depto. de Energia Nuclear-UFPE, CEP: 50740-540 - Recife, PE.
2Centro de Energia Nuclear na Agricultura/USP, C.P. 96, CEP: 13400-970 - Piracicaba , SP.
3Depto. Geologia e Topografia-UFAL, CEP: 57072-970 - Alagoas, AL.
4Depto. de Agronomia-UFU, CEP: 38400-902 - Uberlândia, MG.
5Bolsista do CNPq.
*e-mail: pcotrive[arroba]cena.usp.br
 Página anterior Página anterior |   Voltar ao início do trabalho Voltar ao início do trabalho | Página seguinte  |
|
|
|