 Página anterior Página anterior |   Voltar ao início do trabalho Voltar ao início do trabalho | Página seguinte  |
A partir do estudo do Modelo CERES N (Godwin & Singh, 1998) e identificação dos processos que envolvem a dinâmica de N, foi construído um modelo teórico simplificado, o qual organizou as equações no sistema.
No estudo do ciclo do N em agroecossistemas, para fins de modelagem matemática, além do conhecimento das vias internas de transferência de nitrogênio e de suas taxas, deve-se conhecer as formas de entrada de N no sistema, que são as fontes, e as saídas, ou drenos, do modelo, e a intensidade com que ocorrem. Este modelo matemático que descreve a dinâmica do N no sistema solo cana-de-açúcar, foi construído utilizandose como entradas: fertilizante nitrogenado, palhada remanescente, matéria orgânica já existente no solo, amônia atmosférica e reserva biológica de N. Como saídas de nitrogênio, o modelo considera: remoção pela colheita do N contido nos colmos; lixiviação do nitrato no solo, fora de alcance de exploração do sistema radicular; perdas gasosas de NO, N2O e N2 do solo, mediada por microrganismos anaeróbios desnitrificadores e volatilização da amônia.
O Modelo foi construído no software de simulação STELLA, por ser um software moderno nesta área, completo, com recursos de gráficos, análise de sensibilidade, análise do modelo por partes, fácil visualização do modelo e permite acesso aos dados em planilha Excel. O software STELLA é baseado na metodologia "System Dynamics" desenvolvida na década de 60 por Jay Forrester (Saito & Figueiredo, 2000). O Modelo de Balanço de Nitrogênio completo, construído no software STELLA, pode ser visualizado na Fig. 2.
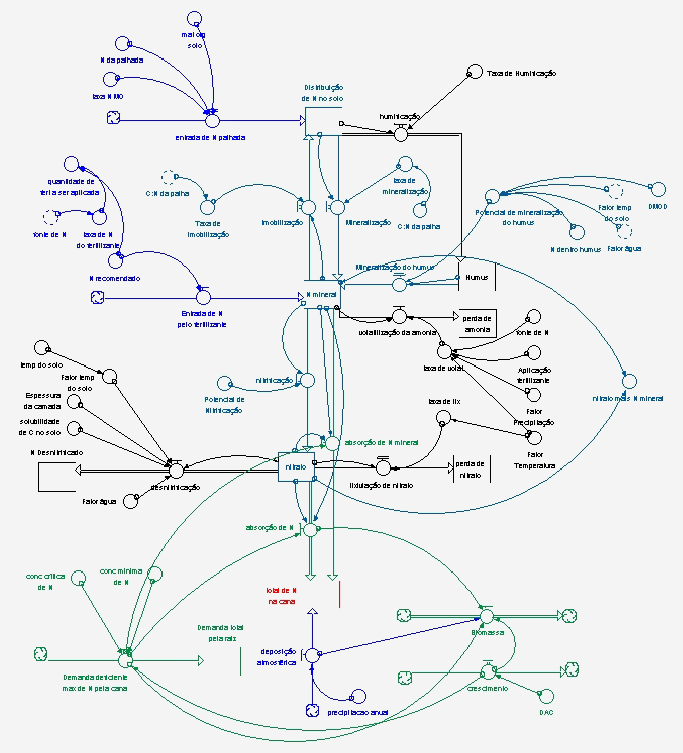
O Modelo de Balanço de N (Fig. 2) está dividido por cores, conforme os caminhos que o nitrogênio percorre no sistema. Os compartimentos e relações que estão em preto indicam as perdas de nitrogênio do sistema; em azul estão as entradas de N; em cinza, o N no solo e os processos que ele sofre; os compartimentos que estão em verde indicam os processos que ocorrem dentro da planta, e em vermelho, o resultado final do modelo, isto é, a quantidade de N na cana-soca.
O Modelo foi então simulado para diversas condições, construindo cenários possíveis nas condições brasileiras, construção de gráficos e interpretação do modelo.
Na simulação de situações que possam vir a ocorrer, ou que são comuns aos produtores, busca-se respostas e auxílio na tomada de decisão quanto ao melhor manejo dos fertilizantes nitrogenados na obtenção do melhor resultado em produção de sacarose da cultura da cana-de-açúcar, com o menor custo possível e menor risco ambiental pela contaminação ocasionada pela lixiviação de nitrato no perfil do solo.
O modelo apresentado foi validado na Usina Costa Pinto, na região de Piracicaba, SP, ainda precisa ser analisado e testado em regiões canavieiras para poder ser utilizado de forma ampla como auxílio na tomada de decisão quanto à fertilização nitrogenada, no Estado de São Paulo.
Foram criados cenários com situações reais que podem ocorrer no campo, nas usinas e destilarias, e foram simulados, através do modelo, os resultados dos parâmetros de saída, os quais estão apresentados nas Tabelas 1, 2 e 3.
No cenário 1 (Tabela 1), ocorreram diferenças significativas nas perdas de N nas três dosagens simuladas (0, 50 e 100 kg ha-1), sendo que com a dose de 100 kg ha-1, que é a recomendada atualmente para a cultura da cana-de-açúcar, as perdas somam-se em 10,1% do teor total de N no sistema; na dosagem de 50 kg ha-1, em 5,2%; e na dosagem zero, essas perdas não chegam a 0,5%. Em estudos de Oliveira (1999), para essas mesmas condições, em cana-soca colhida sem queima prévia, essas perdas chegaram a 10% para a dose de 90 kg ha-1 de N e 7% para a dose de 30 kg ha-1 de N.
Tabela 1.
Cenário 1 - Aplicação de N, fonte uréia, incorporada ao solo, entre os meses de novembro a fevereiro, com precipitação abaixo de 10 mm.
|
Quantidade de N aplicado ao solo |
|||
|
Parâmetros |
0 kg ha-1 |
50 kg ha-1 |
100 kg ha-1 |
|
de N |
de N |
de N |
|
|
kg ha- |
|||
|
Parâmetros de entrada de N |
1 |
||
|
1. Palhada |
50,00 |
50,00 |
50,00 |
|
2. MO do solo |
100,00 |
100,00 |
100,00 |
|
3. Fertilizante |
0 |
50,00 |
100,00 |
|
4. Atmosfera |
37,28 |
37,28 |
37,285. |
|
5. Reserva da cana |
10,00 |
10,00 |
10,00 |
|
Total de entrada |
197,28 |
247,28 |
297,28 |
|
Parâmetros de perda de N |
|||
|
1. N Desnitrificado |
0,09 |
2,06 |
4,82 |
|
2. Perda de amônia |
0 |
0 |
0 |
|
3 Perda de nitrato |
0,48 |
10,76 |
25,24 |
|
Total perdido |
0,57 |
12,82 |
30,06 |
|
Parâmetro de N no solo |
|||
|
1. Húmus |
27,08 |
28,19 |
29,31 |
|
2. MO |
43,67 |
46,17 |
48,67 |
|
3. Nitrato |
0 |
0 |
6,59 |
|
4. N mineral |
9,35 |
9,90 |
10,44 |
|
Total de N no solo |
80,10 |
84,26 |
95,01 |
|
Parâmetro de N na planta |
|||
|
1. N na cana-de-açúcar |
116,61 |
150,20 |
172,21 |
|
Total de N no sistema |
197,28 |
247,28 |
297,28 |
Tabela 2.
Cenário 2 - Aplicação de 100 kg ha-1 de N, em cobertura, entre os meses de novembro a fevereiro, com precipitação abaixo de 10 mm.
|
Fertilizante nitrogenado |
|||
|
Parâmetros |
Uréia |
Uran |
NA e SA1 |
|
kg ha-1 |
|||
|
Parâmetros de entrada de N |
|||
|
1. Palhada |
50,00 |
50,00 |
50,00 |
|
2. MO do solo |
100,00 |
100,00 |
100,00 |
|
3. Fertilizante |
100,00 |
100,00 |
100,00 |
|
4. Atmosfera |
37,28 |
37,28 |
37,28 |
|
5. Reserva da cana |
10,00 |
10,00 |
10,00 |
|
Total de entrada |
297,28 |
297,28 |
297,28 |
|
Parâmetros de perda de N |
|||
|
1. N Desnitrificado |
1,95 |
3,07 |
3,94 |
|
2. Perda de amônia |
82,44 |
48,34 |
22,83. |
|
3. Perda de nitrato |
10,21 |
16,07 |
20,64 |
|
Total perdido |
94,60 |
67,48 |
47,38 |
|
Parâmetro de N no solo |
|||
|
1. Humus |
27,99 |
28,56 |
28,97 |
|
2. MO |
43,21 |
45,39 |
47,10 |
|
3. Nitrato |
0 |
0 |
0 |
|
4. N mineral |
4,76 |
6,85 |
8,66 |
|
Total de N no solo |
75,96 |
80,80 |
84,73 |
|
Parâmetro de N na planta |
1. |
||
|
1. N na cana-de-açúcar |
126,72 |
149,00 |
165,17 |
|
Total de N no sistema |
297,28 |
297,28 |
297,28 |
|
1 NA = Nitrato de Amônio e AS = Sulfato de Amônio. |
|||
Tabela 3.
Cenário 3 - Aplicação de 100 kg ha-1 de N, em cobertura, fonte Uréia.
|
Parâmetros |
Prec1<10mm |
Prec de 10 a 30 mm |
Prec > 30mm |
|||
|
T12 |
T2 |
T1 |
T2 |
T1 |
T2 |
|
|
kg ha-1 |
||||||
|
Parâmetros de entrada de N |
||||||
|
1. Palhada |
50,0 |
50,0 |
50,0 |
50,0 |
50,0 |
50,0 |
|
2. MO do solo |
100,0 |
100,0 |
100,0 |
100,0 |
100,0 |
100,0 |
|
3. Fertilizante |
100,0 |
100,0 |
100,0 |
100,0 |
100,0 |
100,0 |
|
4. Atmosfera |
37,28 |
37,28 |
37,28 |
37,28 |
37,28 |
37,28 |
|
5. Reserva da cana |
10,0 |
10,0 |
10,0 |
10,0 |
10,0 |
10,0 |
|
Total de entrada |
297,28 |
297,28 |
297,28 |
297,28 |
297,28 |
297,28 |
|
Parâmetros de perda de N |
||||||
|
1. N Desnitrificado |
1,95 |
4,87 |
2,83 |
5,31 |
4,82 |
5,79 |
|
2. Perda de amônia |
82,44 |
22,8 |
56,81 |
12,12 |
0 |
0 |
|
3. Perda de nitrato |
10,21 |
2,55 |
14,82 |
2,78 |
25,24 |
3,03 |
|
Total perdido |
94,60 |
30,22 |
74,46 |
20,21 |
30,06 |
8,82 |
|
Parâmetro de N no solo |
||||||
|
1. Húmus |
27,99 |
28,97 |
28,42 |
29,13 |
29,31 |
29,31 |
|
2. MO |
43,21 |
47,10 |
44,84 |
47,83 |
48,67 |
48,67 |
|
3. Nitrato |
0 |
10,13 |
0 |
18,44 |
6,58 |
27,84 |
|
4. N mineral |
4,76 |
8,66 |
6,31 |
9,47 |
10,44 |
10,44 |
|
Total de N no solo |
75,96 |
94,86 |
79,57 |
104,87 |
95,00 |
116,26 |
|
Parâmetro de N na planta |
||||||
|
1. N na cana-de-açúcar |
126,72 |
172,20 |
143,25 |
172,20 |
172,22 |
172,20 |
|
Total de N no sistema |
297,28 |
297,28 |
297,28 |
297,28 |
297,28 |
297,28 |
Quanto ao teor de N na cana, para a dose de 100 kg ha-1 de N, chegou a 172,21 kg ha-1, pois, como pode ser observado na Tabela 1, existem outras fontes de entrada de N no sistema além do fertilizante. Para a dose de 50 kg ha-1 de N foi de 150,20, e para a dosagem zero, foi 116,61 kg ha-1, após período de 360 dias.
Segundo estudos de Gava et al. (2001), o teor de N na cana-soca, após 299 dias, para a dose de 100 kg ha-1 de N, fonte uréia, foi de 172 kg ha-1, valor bem próximo ao encontrado por Coale et al. (1993).
Através da análise do comportamento do N no solo durante o ciclo da cana-de-açúcar, pode-se observar que existe influência da quantidade de fertilizante adicionado ao solo no teor de N como matéria orgânica (MO), pois adicionando-se N ao sistema a atividade dos microrganismos é aumentada, além disso esse N adicionado na forma de fertilizante pode sofrer imobilização e passar a fazer parte da MO do solo, porém, essa influência é pequena. No final do ciclo da cana, ficará no solo, como MO, 16% do N que entrou no sistema para a aplicação de 100 kg ha-1 de N; e ficará 22% do N que entrou no sistema quando não há aplicação de fertilizante. Isso indica que a adição de N no sistema ativa a mineralização da MO. Assim, palhas e outros vegetais celulósicos, se não forem suplementados com nutrientes essenciais, devem ser considerados mais uma fonte de húmus do que como material fertilizante fornecedor de nutrientes para as plantas (Orlando Filho, 1983).
Pode também ser observado nos resultados (Tabela 1), os diferentes comportamentos do N mineral, do nitrato e do húmus nas diferentes dosagens de N simuladas.
A formação de húmus é praticamente igual nos três casos (0, 50 e 100 kg ha-1 de N), porém, na dosagem zero representa 14% e na dosagem 100 kg ha-1 de N, 10% do N total do sistema. O teor de N mineral na dose zero permanece praticamente constante do terceiro mês até o final do ciclo, sem atingir um pico, enquanto o teor de nitrato fica abaixo do N mineral e do húmus.
Na dose 100 kg ha-1 de N, o N mineral tem uma queda mais acentuada que quando aplicado 50 kg ha-1 de N.
Foi criado um outro cenário, onde estão sendo comparadas três fontes diferentes de N, uréia, uran e nitrato de amônio (NA), em aplicação em cobertura, sendo que esta última fonte (NA), no modelo, é considerada igual ao sultato de amônio (SA), e os resultados desse cenário estão apresentados na Tabela 2.
No cenário 2 (Tabela 2), estimou-se através do modelo, perdas de 32% para o fertilizante Uréia, 23% para o Uran e 16% para Nitrato de Amônio ou Sulfato de Amônio.
Oliveira (1999), encontrou perdas de N, utilizando como fonte a uréia, que variaram de 43 a 56% do N total do sistema.
Analisando-se os resultados das simulações do cenário 2 (Tabela 2), nota-se que o comportamento da MO é praticamente igual para os três fertilizantes testados, considerando-se, no modelo, que o nitrato de amônio e sulfato de amônio possuem resultados iguais. O teor de N mineral mostrou uma queda acentuada logo após a aplicação de uréia como fertilizante, e queda mais lenta para aplicação de uran, sulfato de amônio (SA) e nitrato de amônio (NA).
O nitrato atingiu maiores valores quando se utilizou nitrato de amônio ou sulfato de amônio, onde ocorreu também o maior teor de N total na cana, o que ocorreu devido as menores perdas que ocorrem quando se utilizam esses fertilizantes (NA e SA) comparados à uréia e uran em cobertura. A uréia em cobertura volatiliza muito fácil no primeiro mês após aplicação por isso observa-se queda acentuada no N mineral um mês após aplicação do fertilizante, conforme também observou Trivelin (2000), extraindo perdas ainda maiores de amônia quando utilizou uréia em cobertura em experimento. O uran, apesar de volatilizar bem menos que a uréia, também tem uma perda considerável de amônia por volatilização. Quando aplicados incorporados ao solo esses fertilizantes, a perda por volatilização é praticamente zero. A formação de húmus foi semelhante para os três fertilizantes, em torno de 10% do total de N no sistema.
Na Tabela 3 foi simulado outro cenário, onde foram comparados os efeitos da precipitação e da temperatura no momento da aplicação do fertilizante nitrogenado.
No cenário 3, os valores estimados pelo modelo mostram que quando a aplicação do fertilizante é realizada entre os meses março e outubro, as perdas são bem menores comparadas à aplicação realizada nos meses de novembro e fevereiro. As maiores perdas ocorrem quando, no momento da aplicação do fertilizante, a precipitação é menor que 10 mm, e são bem menores quando essa precipitação é superior a 30 mm. Porém, as perdas por lixiviação são maiores com maiores precipitações, e também a desnitrificação, a qual é beneficiada com as chuvas, pois ocorre em condições anaeróbias. Já a volatilização é praticamente nula em altas precipitações, pois o nitrogênio aplicado em superfície, sob a palhada, é levado para camadas mais profundas, não permitindo que volatilize. Nas precipitações até 30 mm no momento da aplicação da uréia, ocorreram maiores perdas de amônia quando aplicados entre os meses de novembro a fevereiro, quando o fator temperatura está beneficiando a volatilização.
O menor teor de N na cana-de-açúcar ocorreu quando a aplicação foi realizada entre os meses de novembro e fevereiro, e a precipitação nessa época era inferior a 10 mm, chegando esse valor a 126,72 kg ha-1 de N. Isso ocorreu devido à grande perda de amônio que ocorreu por ocasião da falta de chuva e da temperatura alta no momento da adubação, reduzindo o teor de N mineral e assim, a nitrificação, ficando baixo teor de N disponível para suprir a demanda de N pela cana. Os maiores valores de N total na cana após doze meses ocorreram quando, no momento em que a cana recebeu fertilizante, a precipitação era superior a 30 mm ou quando a temperatura era mais baixa.
Os resultados encontrados pelo modelo nos três cenários produzidos (Tabelas 1, 2 e 3), mostram que o modelo está estimando valores condizentes com a realidade, conforme experimentos de campo demonstrados por Gava et al. (2001), Trivelin (2000), Trivelin et al. (2002), Coale et al. (1993) e experimento realizado na Usina Costa Pinto, Piracicaba, SP.
Através desses cenários, pode ser concluído que as condições ideais para a cana-de-açúcar, sem considerar custos, são: 1) quando a aplicação do fertilizante for realizada em cobertura (maior facilidade de manejo por causa da palhada sobre o solo), utilizar Nitrato ou Sulfato de Amônio como fonte de N; 2) se, na época de aplicação do fertilizante, a precipitação for alta e/ou a temperatura baixa, aplicar uréia como fonte de N; 3) quando a aplicação for realizada incorporada ao solo, utilizar uréia como fonte de N, porém, essa condição precisa ser estudada para analisar o custo/benefício, pois, em cana-soca coberta com palhada, essa aplicação é bastante trabalhosa.
Na literatura mundial não encontra-se modelos de balanço de nitrogênio para a cultura da cana-de-açúcar, principalmente em relação ao manejo sem queima do canavial. Os modelos que descrevem a dinâmica do nitrogênio para outras culturas, como o CERES N, são difíceis de serem utilizados devido ao grande número de dados de entrada exigidos, dados de difícil medição, que necessitam de experimentos caros e trabalhosos.
Deste modo, o modelo ora apresentado torna-se uma alternativa viável para pesquisadores, técnicos e produtores no entendimento dos processos que envolvem o nitrogênio no sistema e com isso buscarem auxílio a soluções quanto ao melhor manejo de fertilizantes nitrogenados à cultura da cana-de-açúcar, no âmbito das usinas e destilarias.
Esse modelo pode direcionar novas pesquisas nessa área, pois ele indica as "lacunas" de conhecimento e as informações a respeito da dinâmica de N, onde estão faltando dados para torná-lo mais complexo, e dados para validar parâmetros que não foram testados devido a falta de experimentos que buscaram essas informações, ou seja, ajuda na priorização e direcionamento de futuras pesquisas. Ainda, esse Modelo, após serem inseridas novas variáveis, serem testados parâmetros e comprovada sua eficiência, pode ser inserido no software DSSAT, um software de simulação de crescimento de culturas, onde o módulo que executa o crescimento da cultura da cana-de-açúcar (CANEGRO), não possui a rotina que calcula o balanço de nitrogênio.
Assim, esse modelo já testado na região de Piracicaba, SP, após novos testes e validação em outras regiões produtoras de açúcar e álcool, pode servir como um Sistema de Suporte à Decisão confiável nessa área, auxiliando na tomada de decisão quanto a melhor quantidade de fertilizante nitrogenado a ser aplicado na cultura, melhor forma de aplicação, melhor fonte de N, entre outras; dependendo da situação que está sendo analisada.
BARBER, S. A.; CUSHMAN, J. H. Nitrogen uptake model for agronomic crops. In: ISKARDR, K. (Ed.). Modeling waste water renovation land treatment. New York: Wiley Interscience, 1981. p. 382-409.
COALE, F. J.; SANCHES, C. A.; IZUNO, F. T.; BOTTCHER, A. B. Nutrient accumulation and removal by sugarcane growth on everglades histosols. Agron. J., v. 85, p. 310-315, 1993.
GAVA, G. J. de C.; TRIVELIN, P. C. O.; OLIVEIRA, M. W. de; PENATTI, C. P. Crescimento e acúmulo de nitrogênio em cana-de-açúcar cultivada em solo coberto com palhada. Pesquisa Agropecuária Brasileira, Brasília, DF, v. 36, n. 11, p. 1347-1354, nov. 2001.
GODWIN, D. C.; SINGH, U. Nitrogen balance and crop response to nitrogen in upland and lowland cropping systems. In: TSUJI, G. Y.; HOOGENBOOM, G.; THORNTON, P. K. (Ed.). Understanding options for agricultural production. Dordrecht: Kluwer Academic, 1998. p. 55-77.
KEULEN, H. van; WOLF, J. (Ed.). Modelling of agricultural production: weather, soils and crops. Wageningen: Pudoc, 1986. 479 p.
ORLANDO FILHO, J. (Coord.). Nutrição e adubação da cana-de-açúcar no Brasil. Piracicaba: IAA/ Planalsucar, 1983. 369 p.
OLIVEIRA, M. W. Dinâmica de nitrogênio da uréia (15N) no sistema solo-cana-de-açúcar com ou sem queima da palhada. 1999. 93 p. Tese (Doutorado) Centro de Energia Nuclear na Agricultura, Universidade de São Paulo, Piracicaba.
PENNING DE VRIES, F. W. T.; LAAR, H. H. van (Ed.). Simulation of plant growth and crop production. Wageningen: Pudoc, 1982. 308 p. (Simulation Monographs) PEREIRA, A. R. Simulação do crescimento e da produtividade. In: SIMPÓSIO SOBRE MANEJO DE ÁGUA NA AGRICULTURA, 1987, Campinas. Anais. Campinas: Fundação Cargill, 1987. v. 17, p. 201-209.
PESSOA, M. C. P. Y.; LUCHIARI JUNIOR, A.; FERNANDES, E. N.; LIMA, M. A. Principais modelos matemáticos e simuladores utilizados para análise de impactos ambientais das atividades agrícolas. Jaguariuna: Embrapa-CNPMA, 1997. 83 p. (Embrapa-CNPMA. Documentos, 8).
REYNOLDS, J. F. Some misconceptions of mathematical modeling. Plant Physiology, v. 10, n. 11, p. 41-43, 1979.
SAITO, J. R.; FIGUEIREDO, R. S. Uso de simulação baseada em System Dynamics para análise de cadeias agroindustriais. In: WORKSHOP DA SBI-AGRO - SOCIEDADE BRASILEIRA DE INFORMÁTICA APLICADA À AGROPECUÁRIA E AGROINDÚSTRIA, 2., 2000, Campinas. Anais. Campinas: Embrapa Informátaica Agropecuária, 2000. p. 41-46.
STEVENSON, F. J. Cycles of soil: carbon, nitrogen, phosphorus, sulfur, micronutrientes. New York: John Wiley, 1986. 380 p.
STEVENSON, F. J. Nitrogen in agricultural soils. Madison: ASA: SSA, 1982. 940 p.
THORNLEY, J. H. M. Mathematical models in plant physiology: a quantitative approach to problems in plant and crop physiology. London: Academic Press, 1976. 318 p.
TRIVELIN, P. C. O. Utilização do nitrogênio pela cana-de-açúcar: três casos estudados com uso do traçador 15N. 2000. 143 f. Tese (Livre-Docência) Centro de Energia Nuclear na Agricultura, Universidade de São Paulo, Piracicaba.
TRIVELIN, P. C. O.; VITTI, A. C.; OLIVEIRA, M. W.; GAVA, G. J. C.; SARRIÉS, G. A. Utilização de nitrogênio e produtividade da cana-de-açúcar (cana-planta) em solo arenoso com incorporação de resíduos da cultura. Revista Brasileira de Ciência do Solo, Viçosa, MG, v. 26, p. 637-646, 2002.
WIT, C. T. Simulation of living systems. In: PENNING DE VRIES, F. W. T.; LAAR, H. H. van (Ed.). Simulation of plant growth and crop production. Wagninger: Pudoc, 1982. p. 3-8. (Simulation Monographs)
Comunicado Técnico, 28 Embrapa Informática Agropecuária Área de Comunicação e Negócios (ACN) Av. André Tosello, 209 Cidade Universitária - "Zeferino Vaz" Barão Geraldo - Caixa Postal 6041 13083-970 - Campinas, SP Telefone (19) 3789-5743 - Fax (19) 3289-9594 e-mail: sac[arroba]cnptia.embrapa.br 1a edição 2002 - on-line Todos os direitos reservados.
Comitê de Publicacões Presidente: José Ruy Porto de Carvalho Membros efetivos: Amarindo Fausto Soares, Ivanilde Dispato, Luciana Alvim Santos Romani, Marcia Izabel Fugisawa Souza, Suzilei Almeida Carneiro Suplentes: Adriana Delfino dos Santos, Fábio Cesar da Silva, João Francisco Gonçalves Antunes, Maria Angélica de Andrade Leite, Moacir Pedroso Júnior.
Expediente Supervisor editorial: Ivanilde Dispato Normalização bibliográfica: Marcia Izabel Fugisawa Souza Capa: Intermídia Publicações Científicas Editoração Eletrônica: Intermídia Publicações Científicas
Alessandra Fabíola Bergamasco1; Fábio Cesar da Silva2; Luiz Henrique Antunes Rodrigues3; Paulo Cesar Ocheuze Trivelin4
pcotrive[arroba]cena.usp.br
1. Bolsista de Mestrado CAPES, Feagri/Unicamp, Caixa Postal 6011 13083-970 Campinas, SP. (e-mail: afb[arroba]cnptia.embrapa.br)
2. Dr. em Solos e Nutrição de Plantas, Pesquisador da Embrapa Informática Agropecuária, Caixa Postal 6041, Barão Geraldo 13083-970 Campinas, SP. (e-mail: fcesar[arroba]cnptia.embrapa.br)
3. Dr. Prof. Feagri/Unicamp, Caixa Postal 6011 13083-970 Campinas, SP. (e-mail: lique[arroba]agr.unicamp.br)
4. Doutor em Agronomia, Prof. Livre-Docente do Centro de Energia Nuclear na Agricultura (CENA/USP), Caixa Postal 96 13400-970 Piracicaba, SP. (e-mail: pcotrine[arroba]cena.usp.br)
 Página anterior Página anterior |   Voltar ao início do trabalho Voltar ao início do trabalho | Página seguinte  |
|
|
|