
Ahora sí los electrones en los orbitales híbridos sp pueden formar enlaces al compartir electrones con los dos átomos de flúor, debido a que los orbitales híbridos sp son equivalentes uno al otro, pero apuntan en dirección opuesta, el BeF2 tiene dos enlaces s idénticos y una geometría lineal.

Otro tipo muy común de hibridación de orbitales se efectúa cuando un orbital s se
mezcla con los tres orbitales p de la misma subcapa. Por ejemplo, el átomo de carbono
en el metano (CH4) forma cuatro enlaces s equivalentes con los cuatro átomos de
hidrógeno. Podemos imaginar este proceso como el resultado de mezclar el orbital
atómico 2s y los tres 2p del carbono para crear orbitales híbridos equivalentes.
Cada uno de los orbitales híbridos tiene un lóbulo grande que apunta hacia el vértice
de un tetraedro así, dentro de la teoría de enlace valencia se puede describir los enlaces
en el CH4 como el traslape de cuatro orbitales híbridos del C con orbitales 1s de los
cuatro átomos de H

La tabla siguiente muestra la hibridación de orbitales que se produce para alcanzar cada geometría:

Según el tipo de Hibridación la molécula tendrá una orientación y una simetría

Hibridización vs Enlaces
sp3
(Gp:) C
(Gp:) C
(Gp:) C
(Gp:) C
(Gp:) C
(Gp:) C
sp2
sp
SIMPLE
DOBLE
TRIPLE

ISÓMEROS : son compuestos que tienen la misma fórmula molecular, pero difieren en su fórmula estructural o en su geometría espacial; los isómeros difieren al menos en alguna propiedad.
Existen dos tipos fundamentales de isomerismo:
cadena
Estructural posición
(o constitucional) función
ISOMEROS
Geo0metrica: Cis-trans
Estereoisómeros
Enantiómeros
Óptica Diasterómeros

Isómeros
Compuestos con la misma fórmula
pero diferente disposición de los átomos
Isómeros estructurales
Compuestos con diferentes uniones
entre los átomos
Estereoisómeros
Compuestos con las mismas
conexiones entre los átomos, pero
diferente distribución espacial
Isómeros de enlace
Con diferentes enlaces
metal-ligando
Isómeros de ionización
Que producen diferentes iones en disolución
Isómeros geométricos
Distribución relativa:
cis-trans
mer-fac
Enantiómeros
Imágenes especulares

Isomería geométrica
Estereoisomería producida por la diferente colocación espacial de los grupos en torno a un doble enlace
Isomería óptica
Estereoisomería producida por la diferente colocación espacial de los grupos en torno a un estereocentro, habitualmente un carbono quiral
Según el origen o causa de la estereoisomería:

Estas dos formas no son isómeros geométricos ya que la libre rotación del enlace simple convierte una forma en otra (son confórmeros)
ISOMERÍA GEOMÉTRICA
¿Son isómeros geométricos estas dos formas de 1,2 dicloroetano?

Estas dos formas sí son isómeros geométricos ya que el doble enlace no permite la libre rotación. Son las formas trans y cis del 1,2-dicloroeteno
¿Son isómeros geométricos estas dos formas de 1,2 dicloroeteno?

Para que exista isomería geométrica se deben cumplir dos condiciones:
1.- Rotación impedida (por ejemplo con un doble enlace)
2.- Dos grupos diferentes unidos a un lado y otro del enlace

La isomería cis/trans se puede dar también en sistemas cíclicos donde la rotación en torno al enlace simple está impedida
Los isómeros geométricos son diasteroisoméros porque entre ellos no son imágenes especulares

La isomería geométrica tiene efecto sobre las propiedades físicas
1,2-dicloroeteno
2- buteno
El isómero cis tiene un punto de ebullición más alto que el isómero trans
El isómero cis tiene un punto de fusión más bajo que el isómero trans

ISOMERÍA ÓPTICA
Un isómero óptico es aquel que tiene la propiedad de hacer girar el plano de la luz polarizada, hacia la derecha o hacia la izquierda.
Esta propiedad se mide en un aparato llamado polarímetro y se denomina actividad óptica. Si el estereoisómero hace girar la luz hacia la derecha se denomina dextrógiro, y si lo hace girar hacia la izquierda se denomina levógiro.

Esquema de un polarímetro

ISOMERÍA ÓPTICA
Los isómeros ópticos tienen, por lo menos, un carbono quiral.
Un carbono es quiral (o asimétrico) cuando está unido a 4 sustituyentes distintos.
Una molécula es quiral cuando no presenta ningún elemento de simetría (plano, eje o centro de simetría).
Las moléculas quirales presentan actividad óptica.
La quilaridad es una propiedad importante en la naturaleza ya que la mayoría de los compuestos biológicos son quirales.
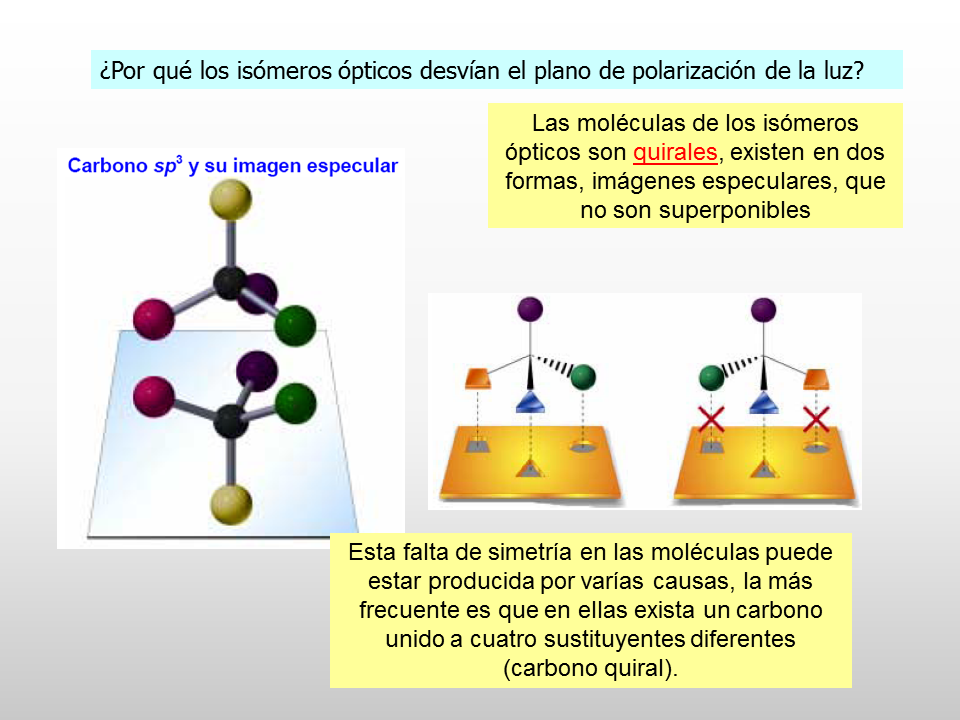
¿Por qué los isómeros ópticos desvían el plano de polarización de la luz?
Las moléculas de los isómeros ópticos son quirales, existen en dos formas, imágenes especulares, que no son superponibles
Esta falta de simetría en las moléculas puede estar producida por varías causas, la más frecuente es que en ellas exista un carbono unido a cuatro sustituyentes diferentes (carbono quiral).

Quiralidad: Es una propiedad según la cual un objeto (no necesariamente una molécula) no es superponible con su imagen especular. Cuando un objeto es quiral se dice que él y su imagen especular son enantiómeros
Presentan plano de simetría

ISOMERÍA ESTRUCTURAL (O CONSTITUCIONAL ) :
Tienen idéntica fórmula molecular, pero difieren entre sí en el orden en que están enlazados los átomos en la molécula
Cadena: Los compuestos se diferencian en la distintas disposición de la cadena de carbonos:
CH3-CH2-CH2-CH3 (C4H10) CH3-CH-CH3
|
CH3
Posición: La presentan aquellos compuestos en que el grupo funcional ocupa diferente posición.
CH3-CH2-CH2OH (C3H8O) CH3-CHOH-CH3
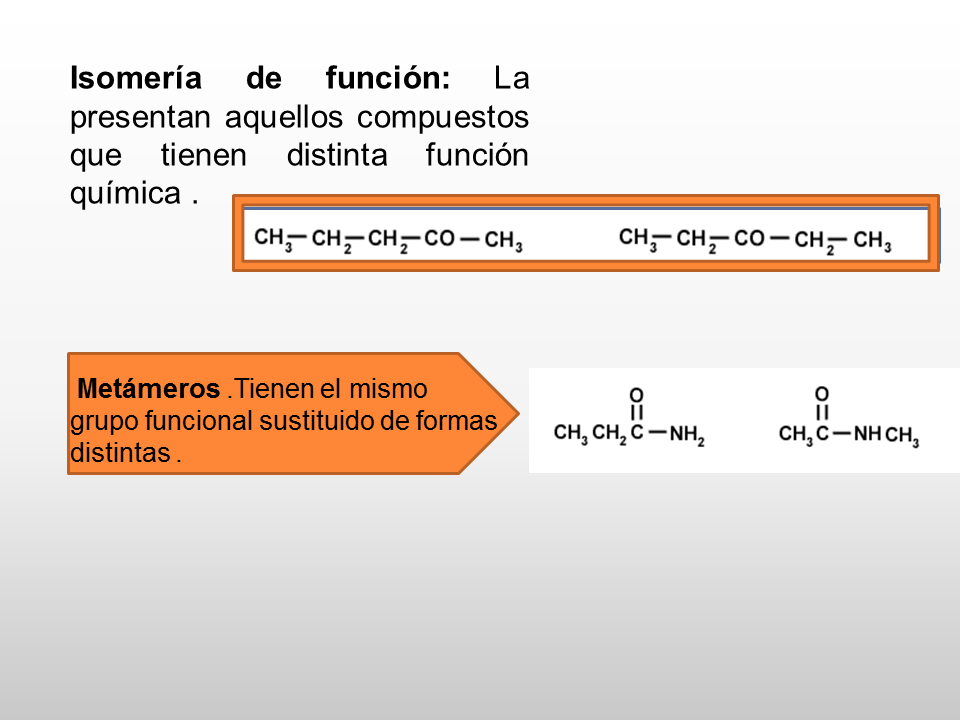
Isomería de función: La presentan aquellos compuestos que tienen distinta función química .
Metámeros .Tienen el mismo
grupo funcional sustituido de formas
distintas .
 Página anterior Página anterior |   Volver al principio del trabajo Volver al principio del trabajo | Página siguiente  |