
Densidad de corriente y velocidad de corrosión
Conocida la densidad de corriente (A/cm2) se puede calcular la velocidad de corrosión teniendo en cuenta la estequiometría y la densidad ?Fe=7.86 g/cm3
Ejemplo: Para una densidad de corriente de 1 A/cm2, calcular la velocidad de corrosión
Masa del equivalente redox=MFe/2=27.93g
Conociendo la densidad ?Fe=m/V=m/(espesor.area) :

Polarización
La diferencia de potencial de electrodo existente antes de que comience el proceso de corrosión, es a circuito abierto, Ec-Ea, es el máximo y este tiende a cero a medida que circula corriente.
A medida que circula corriente comienzan a actuar resistencias del circuito que se oponen a la circulación:
Resistencia propia del electrolito
Resistencia del sistema metálico
Efectos de la polarización: cambios que ocurren como consecuencia del proceso electroquímico en las zonas cercanas a los electrodos
(Gp:) Concentración iónica:
Películas superficiales:
(Gp:) Aumento de cationes
(Gp:) Aumento de aniones
(Gp:) Sólidas
(Gp:) Gaseosas
(Gp:) A(-)
(Gp:) C(+)
(Gp:) A(-)
(Gp:) C(+)
En gral, pequeñas comparadas con la polarización
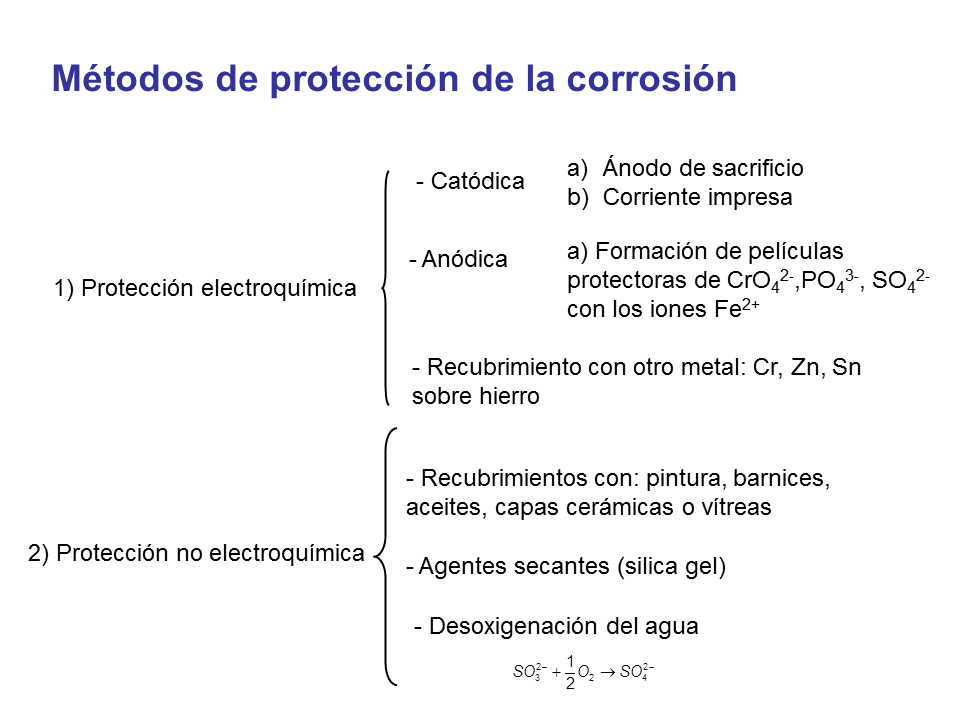
Métodos de protección de la corrosión
1) Protección electroquímica
2) Protección no electroquímica
– Catódica
– Anódica
Ánodo de sacrificio
Corriente impresa
a) Formación de películas protectoras de CrO42-,PO43-, SO42- con los iones Fe2+
– Recubrimientos con: pintura, barnices, aceites, capas cerámicas o vítreas
– Agentes secantes (silica gel)
– Desoxigenación del agua
– Recubrimiento con otro metal: Cr, Zn, Sn sobre hierro

Métodos de protección de la corrosión
Protección Catódica
Ánodo de sacrificio
Zona Catódica C(+):
Zona Anódica A(-):
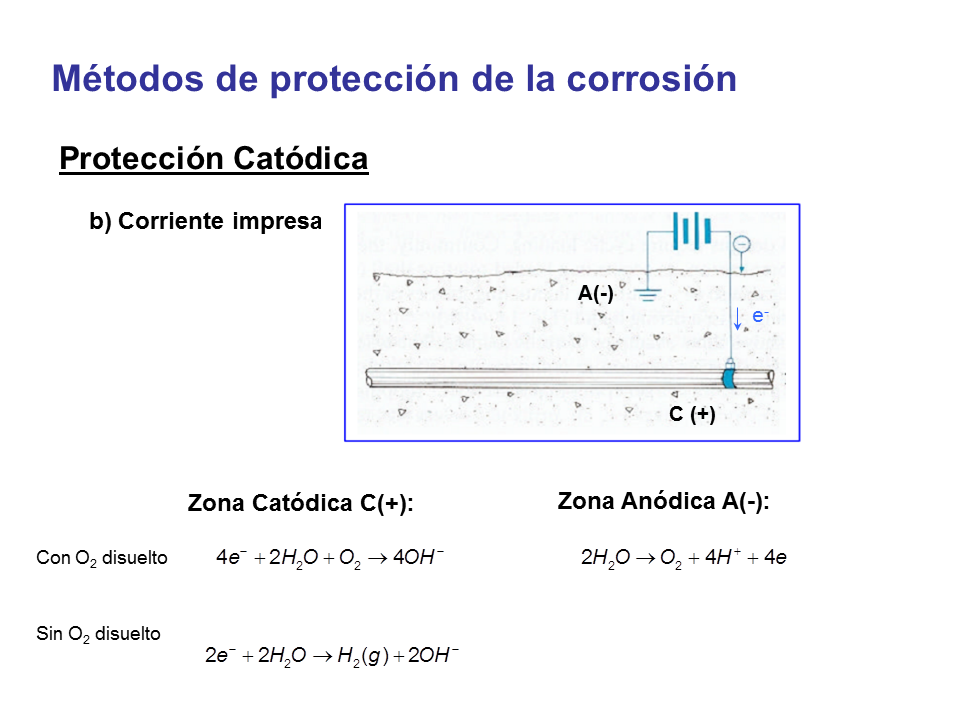
Métodos de protección de la corrosión
Protección Catódica
b) Corriente impresa
Zona Catódica C(+):
Zona Anódica A(-):
Sin O2 disuelto
Con O2 disuelto
e-
C (+)
A(-)

Métodos de protección de la corrosión
Recubrimientos metálicos
Si la cubierta de Sn se perfora, comienza el ataque del Fe porque Eº(Sn)>Eº(Fe)
El Zn, el Cr y Sn forman capas de oxido pasivantes y no se corroen

Métodos de protección de la corrosión
Películas pasivantes
-Formación de películas protectoras `pasivantes de CrO42-,PO43-, SO42- con los iones Fe2+.
Este método es utilizado en la protección de cañerías de hierro, chapas de hierro, perfilería de aluminio (especialmente cromatizado), etc.
Adherentes
Continuas
No porosas
Ocupar el mismo volumen que ocupaba el metal que la originó
Poder restablecerse por sí misma
-Los mismos productos de la reacción de corrosión (óxidos, hidróxidos), pueden ser protectores de la superficie en algunos casos, siempre que cumplan con las siguientes características:
 Página anterior Página anterior |   Volver al principio del trabajo Volver al principio del trabajo | Página siguiente  |