Lípidos
- Definición de
lípidos - Clasificación de
lípidos - Propiedades
físicas de los ácidos grasos - Ceras
- Saponificación
- Detergente
sintético - Oxidación
biológica de los
triglicéridos - Importancia biológica
de los lípidos - Fosfolípidos
- Esteroides
- Lípidos
isoprenoides - Regla de
Ruzicka - Resina de
pino - Resumen
- Bibliografía
Introducción
Definición de lípidos
Los lípidos
son aquellas moléculas orgánicas, denominadas
también biomoléculas, presentes en el tejido de los
animales y las
plantas, los
cuales pueden ser separados o aislados con solventes de baja
polaridad tales como: tetracloruro de carbono,
cloroformo, éter de petróleo, éter etílico,
bencina, benceno, tolueno, mezclas de
benceno o tolueno y etanol en proporción 2:1. Se
encuentran en la madera dentro
de las sustancias extraibles en disolventes poco
polares.
El análisis de estas fracciones ha demostrado
que en el extracto obtenido se encuentran diferentes tipos de
compuestos
orgánicos como son: Ácidos de alta masa
molecular, (denominados ácidos
grasos) Ceras, Triglicéridos, Fosfolípidos,
Glucolípidos, Terpenos, Terpenoides, Esteroles y
Esteroides
Los lípidos pueden clasificarse de acuerdo a su
estructura
química,
aquellos que presentan enlaces éster y pueden ser
hidrolizados, tales como ceras, glicéridos se denominan
lípidos hidrolizables y los que no presentan
enlaces ésteres , denominados no hidrolizables en
los que se encuentran los esteroles, esteroides, terpenos y
terpenoides.
Los lípidos hidrolizables, se clasifican
en: lípidos simples, compuestos, los lípidos
no hidrolizables se clasifican en isoprenoides y
esteroides.
Los lípidos se clasifican en dependencia de las
reacciones
químicas que experimentan , de esta manera aquellos
que reaccionan con disolución de NaOH al 40%, originando
sales, se denominan lípidos saponificables, y los
que no experimentan este tipo de reacción se consideran
lípidos no saponificables.
Los Lípidos se pueden clasificar en dependencia
de las funciones que
realiza en los organismos vivos, encontrando en la naturaleza
aquellos que realizan la función de
reserva y lípidos citoplasmáticos (
presentes en orgánulos celulares, mitocondrias y membrana
celular).
Los lípidos también se clasifican
considerando si aportan ácidos grasos que no son
sintetizados por los organismos animales, los que reciben el
nombre de esenciales; y los no esenciales son
producidos por el metabolismo
animal no necesitan ser ingeridos, son producto del
metabolismo.
Lípidos simples
Los lípidos simples se caracterizan por presentar
la función éster, observe que producto de los
efectos electrónicos presentes en el carbono, el mismo
constituye un centro de baja densidad de
electrones, lo que favorece las reacciones de
sustitución nucleofílica.
Estas reacciones presentan un mayor grado de
complejidad, debido a que los lípidos simples son
compuestos que presentan varios grupos
funcionales, los lípidos simples son abundantes en las
plantas y animales. En las plantas superiores lignificadas se
encuentran en el follaje, la corteza, ramas, semillas, flores,
frutos y madera, ésta última presenta bajos
contenidos de ceras y glicéridos.
Los lípidos simples son abundantes en la
naturaleza en forma de: ceras y glicéridos. Los
glicéridos a su vez se encuentran en forma de grasas y
aceites.
Las ceras son consideradas mezclas de
ésteres de alta masa molecular formadas por ácidos
grasos y alcoholes
monohidroxilados, donde n y m representan el número de
veces que se repite el grupo
CH2, entonces los valores
más frecuentes son: n = 8-18 y
m =16-36.
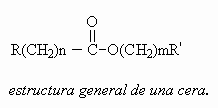
Los glicéridos están constituidos
por ácidos grasos de alta masa molecular y alcoholes
trihidroxilados como el propanotriol, glicerol o
glicerina.
Los glicéridos pueden presentar un grupo
hidroxilo esterificado, denominados monoacilglicérido,
diacilglicérido cuando presentan dos grupos hidroxilos
esterificados y triacilglicérido, cuando se esterificaron
los tres grupos hidroxilos.

Los glicéridos cuando presentan cadenas
carbonadas saturadas reciben la denominación de
grasas, todos los átomos de carbono presentan
hibridación sp3, excepto el carbono del grupo
funcional (éster), por lo que se deduce que los
ácidos grasos presentes en estas estructuras
son de cadenas saturadas.
Los aceites se caracterizan por presentar
instauraciones o sea la presencia de dobles enlaces en las
cadenas de los ácidos grasos que forman la estructura del
glicérido, por tanto no todos los átomos de carbono
presentan hibridación sp3, aparece una nueva
funcionalidad, donde los átomos de carbono presentan
hibridación sp2 y diferente reactividad
química, los ácidos grasos presentes son no
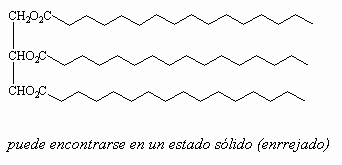
saturados, observe que los ácidos grasos saturados
presentan un empaquetamiento u ordenamiento específico en
las moléculas de triglicérido lo que explica que
las grasas sean
sustancias sólidas, mientras que la estereoquímica
particular de los ácidos grasos que constituyen los
aceites (ácidos grasos no saturados) con isomería
geométrica, siendo más abundante el isómero
cis, proporciona un ordenamiento espacial diferente, lo cual se
puede constatar en las figuras que aparecen a
continuación.

Los lípidos simples son sustancias neutras,
solubles en solventes orgánicos de baja polaridad,
insolubles en agua, con
olores característicos, su consistencia varía desde
líquidos oleaginosos hasta sustancias semi-sólidas
a sólidas.
Sus propiedades tales como acidez y grado de
saturación, facilidad de saponificación
están relacionadas con su estructura química. Estas
propiedades se pueden determinar mediante los siguientes
índices:
Índice de yodo: gramos de yodo que se
adicionan a 100 g de grasa o aceite, mide
el grado de saturación de la grasa o aceite.
Índice de acidez: es el número de
miligramos de hidróxido de potasio que se necesitan para
neutralizar 1 g de grasa o aceite, es una medida de la acidez de
los lípidos simples.
Índice de saponificación:
miligramos de hidróxido de potasio que se necesitan para
saponificar 1 g de grasa o aceite.
Los ácidos presentes en la estructura de los
lípidos simples, son ácidos
monocarboxílicos, presentando un grupo carboxilo y cadenas
que varían en longitud desde 4 hasta 40 átomos de
carbono, siendo los más abundantes en la naturaleza los
ácidos de 16 a 18 átomos de carbono. Los
ácidos se clasifican en saturados y no saturados, son
abundantes en el grano del maíz,
fríjol de soya, grasa humana y animal.
Materia prima | Ac. Palmítico | Ac. Esteárico | Ac. Oleico | Ac. Linoleico |
aceite de maíz | 10 | 5 | 45 | 38 |
aceite de soya | 10 | – | 25 | 55 |
Grasa de puerco | 30 | 15 | 45 | 5 |
Mantequilla | 25 | 10 | 35 | – |
Grasa humana | 25 | 8 | 46 | 10 |
Isomería de los ácidos grasos presentes
en los lípidos simples
Los ácidos grasos no saturados, pueden
presentarse en la naturaleza con una instauración, con dos
o más instauraciones e inclusive pueden presentar otros
grupos funcionales tales como el grupo hidroxilo.
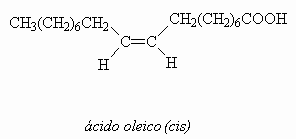
Los ácidos grasos no saturados presentan un doble
enlace entre los átomos de carbono 9 y 10, y esta
instauración es responsable de la presencia de
isómeros geométricos (cis-trans).
Encontrándose estos ácidos en dos formas
diasterómeras diferentes.
En la naturaleza se pueden encontrar con dos y tres
dobles enlaces y los mismos presentan este tipo de
estereoisomería con un mayor grado de
complejidad.

Los ácidos carboxílicos, que se presentan
en la naturaleza, como constituyente de las ceras y los
glicéridos pueden presentar diferentes longitudes de las
cadenas y grupos funcionales diferentes al grupo carboxilo. En la
tabla se muestran la estructura de algunos de ellos.
Ácidos | Átomos de carbono | Estructura |
Saturados | 4 |
|
Caproico | 6 |
|
Caprílico | 8 |
|
Cáprico | 10 |
|
Láurico | 12 |
|
Mirístico | 14 |
|
Palmítico | 16 |
|
Esteárico | 18 |
|
No saturados | 16 |
|
Oleico | 18 |
|
Ricinoleico | 18 |
|
Linoleico | 18 |
|
Linolénico | 18 |
|
Araquídico | 20 |
|
Observe que los ácidos que abundan en la
naturaleza son de números pares de átomos de
carbono, los ácidos insaturados como el palmitoleico,
oleico y ricinoleico presentan una instauración entre el
carbono 9 y 10 (Δ 9). El ácido linoléico
presenta dos instauraciones entre los átomos de carbono 9
y 10, 12 y 13 (Δ9,12). El ácido linolénico
presenta tres dobles enlaces entre los átomos de carbono 9
y 10, 12 y 13, 15 y 16 (Δ9, 12,15). El
αcido araquídico presenta cuatro dobles
enlaces, en los carbonos 9 y 10, 12 y 13, 15 y 16, 18 y 19
(Δ 9, 12, 15,18).
Propiedades físicas de los
ácidos grasos.
Los ácidos grasos presentes en las ceras y los
glicéridos, tienen temperaturas de fusión que
aumentan con el aumento de la masa molecular en el caso de los
ácidos grasos saturados. En el caso de los ácidos
grasos no saturados la temperatura de
fusión disminuye en la medida que aumenta el número
de instauraciones.
Ácidos | Temperatura de fusión |
Caproico | -3 |
Caprílico | 17 |
Cáprico | 31 |
Láurico | 44 |
Mirístico | 58 |
Palmitoleico | 63 |
Estéarico | 70 |
Oleico | 4 |
Linoleico | -12 |
Linolénico | -11 |
Los alcoholes más abundantes en las ceras son los
que presentan de 16 –30 átomos de carbono, observe
que los mismos son alcoholes monohidroxilados con átomos
de carbono par. La temperatura de fusión aumenta con el
aumento de la masa molecular, los alcoholes de cadenas largas se
denominan alcoholes grasos.
Alcoholes | No de carbonos | Temperatura de fusión |
Cetílico | 16 | 49 |
Carnaubílico | 24 | – |
Cerílico | 26 | 79 |
Mirisílico | 30 | 86 |
Las ceras son mezclas de ésteres de alta masa
molecular, constituidas por ácidos grasos y alcoholes
monohidroxilados, son abundantes en la naturaleza, las mismas
pueden ser obtenidas de fuentes
animales y plantas ejemplos de ellas tenemos la cera de abeja, la
cera de carnauba, la lanolina, en los árboles
forestales se puede encontrar la cera del follaje de
conífera y de varios tipos de latifolias.

Las ceras debido a la presencia del enlace éster
experimenta reacciones de sustitución nucleofílica.
La hidrólisis en medio alcalino produce sales de
ácidos grasos y alcoholes monohidroxilados y en un medio
ácido origina ácidos grasos y alcoholes de la misma
naturaleza (monohidroxilados).
La ecuación general que representa la
hidrólisis alcalina de una cera se muestra a
continuación:

Un ejemplo en el cual se puede constatar los productos que
se obtienen de la hidrólisis en medio básico del
palmitato de cetilo se muestra a continuación, sin embargo
esta reacción no es útil para la obtención
de jabones.

La hidrólisis de las ceras es de gran utilidad cuando
se necesita estudiar la composición de los ácidos
grasos y alcoholes presentes en las ceras.


Las reacciones químicas en que participan los
glicéridos han sido ampliamente estudiadas debido a que
presentan un gran valor para la
industria y la
civilización humana.
Baste señalar que la extracción de grasas
y aceites, marcó un precedente importante en la alimentación humana y
su refinación ha constituido un paso de avance para
disminuir los riesgos de
enfermedades por
el consumo de
colesterol presentes en estos materiales
lipídicos. La obtención de jabón
constituyó un avance importante en la salud humana, en la higiene y
riesgo a
contraer enfermedades.
Reacciones de los glicéridos
La hidrólisis de los triglicéridos se
produce mediante la escisión del enlace éster, y la
formación de ácidos y glicerina.
Ecuación general de
hidrólisis ácida de un
triglicérido

La hidrólisis enzimática se produce
en presencia de catalizadores biológicos (enzimas lipasas).
En los animales se producen en el estómago y el intestino.
En los vegetales y plantes superiores lignificadas, las enzimas
lipasas tienen su máxima actividad en el proceso de
germinación de las semillas oleaginosas.
Ecuación general de
hidrólisis enzimática de un
triglicérido

triglicérido glicerol
ácido graso
Un ejemplo de la hidrólisis de los
triglicéridos en presencia de enzimas lipasas puede ser
representado por la siguiente ecuación
química.

El jabón es una mezcla sales de metales alcalinos
(usualmente sales de sodio), provenientes de ácidos de 16,
a 18 átomos de carbono, pero pueden contener sales de
sodio de ácidos carboxílicos de baja masa
molecular.
Se estima que el jabón fue descubierto por los
fenicios,
otros atribuyen este descubrimiento a los antiguos egipcios; se
supone que data del año 600 A.C., se conoce también
que tribus teutónicas hacían el jabón pero
se desconocía su acción
limpiante, estos datos fueron
publicados por Julio Cesar, no obstante estos descubrimientos
fueron olvidados, no fue hasta el Renacentismo que el
jabón fue redescubierto. Su utilización con los
fines actuales data del siglo XVIII.
La preparación o manufactura
del jabón no ha variado mucho, se usan las mismas técnicas
que antiguamente, se trata la grasa o aceite con
disolución de NaOH al 40%, mediante la reacción
conocida como Saponificación, entonces se produce la
hidrólisis de los triglicéridos formando
ácidos grasos y glicerol o glicerina los ácidos se
convierten en sales en presencia de una base.

triglicérido glicerol sal de
ácidos grasos
Ecuación general de
saponificación de un
triglicérido

Los aceites se saponifican originando mezclas de sales
de ácidos grasos insaturados y la glicerina.

En la antigüedad cuando no se conocía la
sosa (NaOH), se utilizaba cenizas de madera las cuales contienen
potasio en forma de carbonatos (K2CO3), y
estas sales proporcionaban el medio alcalino para producir la
reacción de saponificación.
Para completar esta reacción, en ocasiones se
adicionan sales para favorecer la precipitación del
jabón y el glicerol se recupera mediante destilación. El glicerol es utilizado en la
industria cosmética, para disminuir la humedad del
tabaco y en la
industria farmacéutica.
El jabón es purificado en agua a la temperatura
de ebullición, precipitado, secado en moldes, adicionados
varios aditiv os, como perfumes, sustancias medicinales,
bactericidas etc.
Las moléculas de la sal de sodio de los
ácidos grasos, o sea, el jabón presenta
acción limpiante debido a su estructura química,
las mismas son largas cadenas de hidrocarburos
que presentan un enlace iónico entre el anión
carboxilato y el sodio, lo que le proporciona un carácter hidrófilo (afinidad por
el
agua).
Como resultado él se disuelve en agua, sin
embargo la cadena hidrocarbonada es no polar y por tanto
hidrófoba (no tiene afinidad por el agua), estos dos
efectos contrarios hace que el jabón sea atraído
por las grasas y por el agua y dice de sus acción
limpiante. Las partículas del jabón son suspendidas
en el agua formando micelas de 50 a 150 moléculas, donde
las cadenas hidrocarbonadas se ordenan y el grupo funcional queda
expuesto al agua, según esquema II.

Esquema I.
El jabón actúa como un surfactante
disminuyendo la tensión superficial del agua, su
acción se debe a que las cadenas de hidrocarburo de las
moléculas del jabón se disuelven en sustancias poco
polares, tales como gotitas de aceite o grasa y la parte
iónica de la molécula es atraída por el agua
según el esquema III.
Se podrá observar que se produce entonces una
repulsión entre estos agregados moleculares, debido a la
presencia de cargas iguales y es por esto que las
partículas de jabón no colapsan y se encuentran
suspendidas en la disolución.

Esquema II.
La principal desventaja de los jabones es que precipita
con el agua dura (agua que contiene iones Ca2+ ;
Mg2+; Fe2+), debido a que la sal del
ácido puede intercambiar el ión sodio por el
calcio, según la siguiente ecuación.

Reacciones químicas de los glicéridos
no saturados.
Los aceites experimentan los mismos tipos de
reacción que las grasas, excepto la hidrogenación
catalítica al doble enlace carbono-carbono para producir
grasas. Esta reacción presenta gran importancia desde el
punto industrial debido a la conversión de aceites en
grasas, proceso conocido como endurecimiento de los aceites, lo
que permite el mejor almacenaje y
transportación.

La hidrólisis de un triglicérido no
saturado origina la formación de glicerol y ácidos
grasos no saturados, cuando se produce la reacción en
medio básico en presencia de NaOH o KOH, entonces se
produce la formación de sales de ácidos grasos no
saturados o jabones.

Los detergentes sintéticos comenzaros a
utilizarse después de la II guerra mundial y
la estructura química es muy diferente a la del
jabón (sales sódicas de ácidos grasos), los
mismos son sulfonatos o sulfatos de sodio de cadenas largas (doce
o más átomos de carbono); los mismos presentan las
ventajas de no precipitar con los iones metálicos
presentes en el agua dura.

Los jabones y detergentes pertenecen al grupo de
compuestos conocidos como surfactantes; los cuales pueden
disminuir la tensión superficial del agua, pero deben
presentar una parte de la molécula hidrófoba (
varias cadenas de hidrocarburos) y una terminación
hidrofílica (usualmente, pero no necesariamente
iónica).
Los surfactantes pueden ser clasificados en
aniónicos, catiónicos o neutrales en dependencia de
la naturaleza de los grupos hidrofílicos. Los jabones son
surfactantes aniónicos debido al la presencia del
anión carboxilato, un ejemplo de surfactante
catiónico es el cloruro de benzalconio (cloruro de
N-bencil amonio cuaternario). Los surfactantes neutrales
contienen grupos polares los cuales pueden interactuar con el
agua a través de los enlaces por puente de hidrógeno.




Los surfactantes disminuyen la tensión
superficial del agua debido a que destruyen los enlaces de
hidrógeno en la superficie del agua, esto es debido a la
posición que ocupan las cabezas hidrofílicas sobre
la superficie del agua y sus colas hidrofóbicas se
extienden fuera de la superficie del agua.
Oxidación biológica de los
triglicéridos
La oxidación biológica de las
grasas es un proceso que se produce en las plantas y animales
en la cual se obtiene energía metabolicamente aprovechable
para los procesos que
se requieren en el organismo animal o vegetal, la misma se
diferencia de las reacciones que se practican en el laboratorio es
una reacción bioquímica
que ocurre a nivel celular. Por tanto se entenderá que los
catalizadores usuales en estas transformaciones se diferencian de
los vistos en el Tema II, son catalizadores biológicos
denominados enzimas, para reconocer que se trata de una
enzima observe que presenta la terminación
asa.
El proceso de degradación u oxidación
biológica, también conocido como β-
oxidación, se reconoce en bioquímica como el
proceso de catabolismo.
El catabolismo de las grasas y aceites
(triglicéridos), comienza con la hidrólisis para
formar glicerol y ácidos grasos, ocurre en el
estómago y en los intestinos de los animales y el hombre. El
glicerol sigue una ruta metabólica en la cual es
fosforilada para obtener monofosfato de glicerilo con posterior
oxidación produciendo gliceraldehído- 3-
fosfato.
Los ácidos grasos son catabolizados mediante el
proceso de la β- oxidación que consta de cuatro
etapas y este proceso se produce repetitivamente hasta
degradación total de la molécula, produciendo
acetilCoA.
Etapas de la β-
oxidaciσn:
- Dos átomos de hidrógeno provenientes de
los carbonos 2 y 3 son removidos para formar el éster
α,β-insaturado. Esta es una
reacciσn de deshidrogenación u
oxidación que ocurre en presencia de la enzima
acilCoAdeshidrogenasa. - Se produce la adición de agua al doble enlace
carbono- carbono, para producir el éster β-
hidroxilado. La enzima que interviene en el proceso es la
enoilCoAhidrolasa. - Ocurre una oxidación del grupo hidroxilo del
carbono β, obteniéndose el β-cetoacilCoA, en
presencia de la enzima L-3-
hidroxiacilCoAdeshidrogenasa. - La ruptura de la cadena, que se produce por átomo de
carbono β, origina el acetilCoA y un
αcido de dos átomos de carbono menos
el cual origina acilCoA cuando interviene otra molécula
de la CoA
Importancia biológica de los
lípidos
Los lípidos simples como las ceras presentan gran
importancia en las plantas ya que cumplen funciones tales como
recubren las hojas para evitar la transpiración y evitan
el ataque de plagas y enfermedades cuando se encuentran en la
corteza de las diferentes especies forestales.
Los glicéridos forman parte de la doble membrana
que recubre las células
animales, forman el tejido adiposo en los animales y el hombre
constituyendo un material de reserva y constituyen fuentes de
ácidos grasos esenciales para la alimentación,
mediante su degradación o catabolismo reportan
energía metabolicamente aprovechable en forma de ATP (
trifosfato de adenosina )
Los fosfolípidos son lípidos
hidrolizables, debido a que contienen la función
éster y son lípidos compuestos debido a que rinden
por hidrólisis glicerol, ácidos orgánicos
grupos fosfatos y otros compuestos. Estos compuestos usualmente
contiene dos grupos ésteres formado por ácidos
grasos y un enlace éster con el grupo fosfato en el
átomo de carbono tres.
La particularidad de los fosfoglicéridos es que
sus moléculas contienen dos largas cadenas
hidrofóbicas y un grupo hidrofílico altamente polar
(un grupo que constituye un ión dipolar). Los
fosfoglicéridos son por esta razón surfactantes
neutrales.

L-lecitina L-cefalina
Observe que en las estructuras anteriores los enlaces
ésteres de los átomos de carbono uno y dos las
cadenas están ubicadas en posiciones contrarias,
presentando una estereoquímica particular, el átomo
de carbono dos es un centro estereogénico y las
moléculas de lecitina y cefalina son disimétrica y
por tanto moléculas quirales las cuales presentan
actividad óptica
y de acuerdo a su estructura se designa serie L para estos
compuestos.
Observe que R y R’son radicales acilos que
presentan de 12 a 20 átomos de carbono y el grupo fosfato
enlazados al átomo de carbono 3, unido a una amina como la
colina.
La lecitina y cefalina son dos tipos de
fosfoglicérido que se encuentran principalmente en el
cerebro, en las
células nerviosas, en el hígado, yema de huevo,
germen de trigo, levadura soya y otros compuestos.
Los esteroides son lípidos no hidrolizables, no
saponificables en general, que contienen una estructura
química muy particular, presentando cuatro anillos
condensados, designados por A, B, C, D. Los átomos de
carbono son enumerados como se muestra en la estructura
siguiente.

Muchos esteroides pueden ser considerados como derivados
del colestano. Observe que en esta estructura aparece la
estructura base del perhidrociclopentanofenantreno.
Los esteroides pueden ser encontrados en casi todos los
tejidos de los
organismos vivos. Muchos esteroides actúan como hormonas en
animales y el hombre.
Dentro del grupo de esteroides el colesterol es un
importante componente de las membranas celulares en los animales
superiores y es un intermediario necesario en la biosíntesis de hormonas esteroidales. Sin
embargo este puede ser sintetizado a partir del acetil coenzimaA,
y no es necesario como suplemento en la dieta. Altos niveles de
colesterol en sangre
está asociado con la ateroesclerosis (endurecimiento de
las arterias).
Otros esteroides, como la cortisona y cortisol son
ampliamente utilizados para el tratamiento de la inflamación debida a procesos
alérgicos o artritis reumatoidea.
Los andrógenos, estrógenos y progesterona
son compuestos esteroidales, así como los ácidos
biliares. Cumpliendo funciones de regulación sexual,
reproductivo y en caso de este último, se combina con
sales de sodio de la glicina en el intestino los que propician la
formación de agente emulsificantes, facilitando la
digestión.

Los lípidos isoprenoides se clasifican en
terpenos y terpenoides, considerándose como derivados del
isopreno, sin embargo ellos son divisibles en unidades de
isopreno, de forma natural ellos se biosintetizan en las plantas
a partir del pirofosfato de isopentenilo. Son abundantes en las
plantas, en la actualidad se conocen alrededor de 22 000
compuestos diferentes, aunque existen muchos de estructuras
desconocidas.
Características
estructurales. Terpenos y terpenoides
Los compuestos terpénicos son sustancias
extraparietales, que no constituyen parte de la pared celular,
obtenidas del tejido de los vegetales y plantas superiores
lignificadas, con solvente de baja polaridad; constituyen la
fracción lipídica no hidrolizable, sin embargo
algunos de ellos pueden saponificarse para obtener sales de
sodio. Desde el punto de vista químico son estructuras
derivadas del
2-metil 1,3- butadieno (isopreno).
Los lípidos isoprenoides se clasifican en
terpenos y terpenoides. Los terpenos son hidrocarburos saturados
y no saturados, cíclicos y acíclicos, mientras que
los terpenoides poseen cadenas hidrocarbonadas pero exhiben la
presencia de grupos funcionales (hidroxilo, carbonilo,
carboxilo), las cadenas pueden ser cíclicas y anillos
condensados).
Regla isoprénica: Toda sustancia de origen
vegetal con un número de átomos de carbono
múltiplos entero de cinco, con toda probabilidad es
divisible en unidades de isopreno.
Terpenos | Unidades de isopreno | Número de átomos de |
Monoterpenos | 2 | 10 |
Sesquiterpenos | 3 | 15 |
Diterpenos | 4 | 20 |
Sesterpenos | 5 | 25 |
Triterpenos | 6 | 30 |
Tetraterpenos | 8 | 40 |
Politerpenos | > 8 | > 40 |
Los terpenos se clasifican en dependencias de las
unidades de isopreno.
La estructura de los terpenos y terpenoides se forma
mediante la unión de unidades de isopreno, estas uniones
pueden ser: cabeza-cabeza (uniones 1-1), cabeza-cola, (uniones
1-4), cola-cola (uniones 4-4).


cabeza mirceno

Monoterpeno
Monoterpenoides.


Sesquiterpeno
Una de las fuentes principales de terpenos y terpenoides
es la resina de los pinos, exudados arbóreos que se
producen cuando se practican incisiones en la corteza de estas
especies. Las resinas u oleorresinas son una mezcla de
ácidos resinosos (ácidos diterpenoicos) disueltos
en una mezcla de hidrocarburos terpénicos.
Mediante la destilación con arrastre con vapor de
la resina de los pinos se obtiene una fracción
volátil conocida como aceite de trementina o
aguarrás, que incluye hidrocarburos terpenos
y terpenoides tales como, α-pineno, β-pineno, mirceno,
limoneno, farneseno, β-felandreno,
Δ3-careno, borneol,
canfeno, terpinoleno, metilcarvinol, p-cimol,
longuifoleno.
En Cuba existen
cuatro especies de pinos: Pinus caribaea, Pinus tropicalis,
Pinus cubensis y Pinus maestrensis, estudios
realizados han demostrado que contienen altos contenidos de
α-alfa pineno (monoterpeno de 10 αtomos
de carbono y pequeñas cantidades porcentuales de los
demás compuestos terpénicos).
Especies de pinos | Contenido de α- |
Pinus tropicalis | 93,2 – 96,9 % |
Pinus occidentalis | 87,1 – 94,1 % |
Pinus cubensis | 76,6 – 88,6 % |
Pinus caribaea | 67,3 – 91,0 % |
Las especies de Pinus tropicalis, occidentalis y
cubensis además presentan β- pineno y cantidades
porcentuales muy pequeñas de los demás terpenos,
mientras que el Pinus caribaea presenta altos contenidos de
β- felandreno.
La resina de los pinos son mezclas de compuestos
terpénicos, cuando se destila la resina se obtienen dos
fracciones, una fracción volátil conocida como
aceite de trementina formada por monoterpenos y monoterpenoides y
una fracción no volátil conocida como pez rubia o
colofonia
La oleorresina contiene de 16-20 % de aceite de
trementina y de 64-70 % de colofonia.
Los terpenos y terpenoides son los encargados de
impartir olor, color, sabor y
resistencia al
ataque de microorganismos e insectos a la madera de especies
forestales.
La colofonia se obtiene como residuo sólido de la
destilación de la resina es una mezcla de ácidos
diterpenoicos tales como: ácido abiético,
ácido neobiético, ácido
dehidroabiético, ácido pimárico,
dextropimárico, levopimárico y ácido
palústrico.
La colofonia contiene ácido abiético
(15-20 %), ácido neoabiético (15-20 %),
ácido levopimárico (30-35 %) y ácido
pimárico (16 %). La composición varía en
dependencia del método de
separación o sea si se destila la resina o si se obtienen
los ácidos a partir del licor negro de los procesos de
pulpeo.

Usos de la trementina
- Desinfectante
- Aromatizantes
- Disolvente en la industria de pinturas y
barnices - Sustancias humectantes (con baja tensión
superficial). - Dispersante de pigmentos debido a que es una
sustancia apolar en pinturas. - Se utiliza como sustancia secante.
Usos de la colofonia
- Fabricación de colas papeleras
para unir las fibras celulósicas. Estas mezclas de
ácidos resínicos se tratan con NaOH,
produciéndose la reacción de
saponificación , obteniendo sales sódicas de los
ácidos diterpenoicos. - Las colofonias y sus derivados se utilizan en la
producción de sustancias tensoactivas,
gomas de mascar, compuestos cerosos para el recubrimiento de
cítricos para evitar la maduración
excesiva.
Las ceras son mezclas de ésteres simple de alta
masa molecular, sólidos cerosos; mientras que los aceites
y grasa son triglicéridos formados por la
esterificación del glicerol con ácidos grasos de
cadena larga (siendo los más abundantes entre 16 y 18
átomos de carbono). Los aceites son lípidos
oleaginosos formados por ácidos grasos no saturados, los
mismos contienen átomos de carbono par e isomería
geométrica cis- trans alrededor del doble enlace, siendo
los diasterómeros cis los más abundantes en la
naturaleza. Las grasas son semisólidas o sólidas
con ácidos grasos saturados.
El jabón consiste en una mezcla de sales de sodio
o potasio de ácidos grasos, que se producen cuando se
tratan los triglicéridos con disolución acusa de
NaOH o KOH estas sales son surfactantes, disminuyendo la
tensión superficial del agua, presentando acción
limpiante. Otros surfactantes son sulfonatos o sulfatos que
contienen largas cadenas hidrocarbonadas.
Los fosfoglicéridos tales como lecitina y
cefalina contienen glicerol esterificado con dos moléculas
ácidos graso y la fosfatidilamina, presentando un centro
estereogénico, siendo moléculas quirales que
pertenecen a la serie L.
El colesterol, cortisona y ácidos biliares son
esteroides que contienen el sistema de
anillos condensados del
ciclopentanoperhidrofenantreno.
Los terpenos son hidrocarburos divisibles en unidades de
isopreno, mientras que los terpenoides exhiben grupos funcionales
presente en sus moléculas; tales como; hidroxilo,
carbonilos y carboxilos. Son abundantes en la naturaleza y muchos
de ellos son responsables del olor, color y resistencia al ataque
de microorganismos e insectos en la madera de las plantas
superiores lignificadas. Una fuente fundamental de terpenos y
terpenoides son las resinas de los pinos.
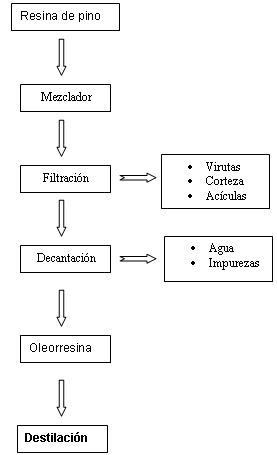
Diagrama de flujo para el proceso de
destilación de la resina
- Fessenden Ralf j., Fessenden Joan. S, Organic
Marshall W. Logue. An International Thomson Publishing.
Company, 1998. - Mc. Murry John. Organuc chemistry JTP. An
International Thomson Publisking Compary 1984. - Solomons, G."Química Orgánica"
University of South Florida 1997.
Autor:
Lic. Química Yasiel Arteaga
Crespo
Dra. Ciencias
Técnicas Leila R. Carballo Abreu