1.
Introducción
2. Fabricación de
vidrio
3. ¿Cómo y con qué se
hace el vidrio?
5. Vidrio soluble y vidrio
sodocálcico
6. Vidrio al plomo
7. Vidrio de
borosilicato
8. Color
9. Ingredientes
diversos
10. Propiedades
físicas
11. Mezcla y
fusión
12. Moldeado
13. Vidrio tensionado
14. Tipos de vidrio
comercial
15. El talco
Vidrio sustancia amorfa fabricada sobre todo a partir de
sílice (SiO2) fundida a altas temperaturas con boratos o
fosfatos. También se encuentra en la naturaleza, por
ejemplo en la obsidiana, un material volcánico, o en los
enigmáticos objetos conocidos como tectitas. El vidrio es una
sustancia amorfa porque no es ni un sólido ni un
líquido, sino que se halla en un estado
vítreo en el que las unidades moleculares, aunque
están dispuestas de forma desordenada, tienen suficiente
cohesión para presentar rigidez mecánica. El vidrio se enfría hasta
solidificarse sin que se produzca cristalización; el
calentamiento puede devolverle su forma líquida. Suele ser
transparente, pero también puede ser traslúcido u
opaco. Su color
varía según los ingredientes empleados en su
fabricación.
El vidrio fundido es maleable y se le puede dar forma
mediante diversas técnicas.
En frío, puede ser tallado. A bajas temperaturas es
quebradizo y se rompe con fractura concoidea (en forma de concha
de mar).
Se fabricó por primera vez antes del 2000 a.C., y
desde entonces se ha empleado para fabricar recipientes de uso
doméstico así como objetos decorativos y
ornamentales, entre ellos joyas. (En este artículo
trataremos cualquier vidrio con características comercialmente
útiles en cuanto a trasparencia, índice de
refracción, color.
El vidrio se fabrica a partir de una mezcla compleja de
compuestos vitrificantes, como sílice, fundentes, como los
álcalis, y estabilizantes, como la cal. Estas materias
primas se cargan en el horno de cubeta (de producción continua) por medio de una
tolva. El horno se calienta con quemadores de gas o petróleo.
La llama debe alcanzar una temperatura
suficiente, y para ello el aire de combustión se calienta en unos
recuperadores construidos con ladrillos refractarios antes de que
llegue a los quemadores. El horno tiene dos recuperadores cuyas
funciones
cambian cada veinte minutos: uno se calienta por contacto con los
gases
ardientes mientras el otro proporciona el calor
acumulado al aire de combustión. La mezcla se funde (zona
de fusión)
a unos 1.500 °C y avanza hacia la zona de enfriamiento,
donde tiene lugar el recocido. En el otro extremo del horno se
alcanza una temperatura de 1.200 a 800 °C. Al vidrio
así obtenido se le da forma por laminación o por
otro método.
Materiales y técnicas.-
El ingrediente principal del vidrio es la sílice, obtenida
a partir de arena, pedernal o cuarzo.
3. ¿Cómo y con
qué se hace el vidrio? .-
Además del papel que ha
desempeñado en la vida cotidiana, el vidrio ha tenido una
trascendental participación en el desarrollo de
la tecnología y de nuestra concepción
de la naturaleza. Gracias a él sabemos cómo son los
microorganismos, a través del microscopio;
cómo es el Universo, con
el uso de los telescopios; cuál es la naturaleza del
átomo y
el dinamismo de una célula
viva. La variedad de usos que se le ha encontrado solamente
estб limitada por la capacidad y el ingenio
del hombre. Su
versatilidad es difнcilmente sustituible, por lo que su
estudio se vuelve mбs interesante.
Básicamente, el principio de fabricación
del vidrio ha permanecido invariable desde sus comienzos, pues
las principales materias primas y las temperaturas de
fusión no han sido modificadas. Sin embargo, las
técnicas se han transformado para conseguir un proceso de
producción más acelerado, y los investigadores han
elaborado diferentes compuestos para combinarlos con el material
bruto y así variar las propiedades físicas y
químicas, de manera que sea posible disponer de una amplia
gama de vidrios para diversas aplicaciones.
El vidrio se hace en un reactor de fusión, en
donde se calienta una mezcla que casi siempre consiste en arena
silícea (arcillas) y Óxidos metálicos secos
pulverizados o granulados. En el proceso de la fusión
(paso de sólido a líquido) se forma un
líquido viscoso y la masa se hace transparente y
homogénea a temperaturas mayores a 1 000 grados
centígrados. Al sacarlo del reactor, el vidrio adquiere
una rigidez que permite darle forma y manipularlo. Controlando la
temperatura de enfriamiento se evita la desvitrificación o
cristalización.
En la antigüedad la fusión se hacía
en moldes de arena hechos en casa, como se ve en la figura 8,
pero para la industrialización de este proceso fue
necesario construir grandes hornos (figura 9), donde
además de las materias primas se podrán
añadir trozos de vidrio viejo de desecho.
Figura 8. Horno de fusión casero antiguo (siglo XVII).
Figura 9. Horno tanque.
Durante los tiempos primitivos de la industria del
vidrio, las únicas materias primas que se utilizaban en su
fabricación eran las arcillas. Hoy en día se
emplean distintas mezclas para
obtener diferentes tipos. Por ejemplo, los bloques de vidrio se
fabrican en moldes con una mezcla de arena de sílice, cal
y sosa, y se les añade dolomía, arcilla de aluminio y
productos para
el refinado. En la actualidad muchos materiales
desempeñan un papel importante, pero las arcillas siguen
siendo fundamentales.
Aunque la palabra puede resultarnos conocida, es posible
que no sepamos que la arcilla es el producto del
envejecimiento geológico de la superficie de la Tierra, y
que como esta degeneración es continua y se produce en
todas partes, es un material terroso muy abundante en la
naturaleza. De hecho, para el cultivador, el minero o el
constructor de carreteras resulta un estorbo.
Las rocas
ígneas primarias que dieron lugar a las arcillas fueron,
entre otras, granitos, pegmatitas y feldespatos. El
envejecimiento de estas rocas primarias fue producido por la
acción mecánica del agua, el
viento, los glaciares y los movimientos terrestres, combinados
con la acción química del agua y
del bióxido de carbono a
altas temperaturas. Hoy en día las mismas fuerzas
naturales siguen produciendo arcilla,
formбndose asн mбs cantidad de la
que el hombre puede utilizar.
La arcilla es un material engañosamente sencillo.
No tiene la obstinada dureza de la piedra, ni la fibra
temperamental de la madera, ni la
solidez del metal, pero tiene una fragilidad y una inconstancia
que parecen pedir un cuidado especial. Es blanda, dócil,
plástica, maleable, sin veta ni dirección. Clasificarla es una tarea
difícil y conduce a diferentes resultados, dependiendo de
la característica del material que se tome como
referencia. La podemos ordenar desde un punto de vista
geológico, mineralógico o de acuerdo con su
uso.
Una clasificación geológica es la
más conveniente en el caso de la arcilla, pues puede ser
una guía preliminar útil de las materias primas
empleadas en la industria del vidrio (figura 11). Asimismo
pueden dividirse en dos grandes grupos: las
primarias y las secundarias. Las arcillas primarias,
tambiйn conocidas como arcillas residuales, son las que se
han formado en el lugar de sus rocas madres y no han sido
transportadas por el agua, el
viento o el glaciar. Al no haber movimiento,
casi no hay oportunidad de que las mezclas de otras procedencias
alteren su composición, por lo que tienden a ser
relativamente puras y libres de materiales no arcillosos. Son
valoradas por su limpieza, su blancura, su suavidad, su bajo
costo y su
dificultad para encontrarlas. Las arcillas secundarias son
aquellas que han sido desplazadas del lugar donde fueron
formadas. Son mucho más comunes, menos puras, pues tienen
material procedente de distintas fuentes, y su
composición varía ampliamente. Estos datos son
particularmente importantes para las personas que van a utilizar
estos materiales, ya que las condiciones de trabajo se alteran de
manera notable. Las arcillas que se encuentran esencialmente
puras requieren un tratamiento mínimo, mientras que las
otras tienen que tratarse a profundidad antes de ser utilizadas
en la industria.
Figura 11. Diagrama de flujo
de la clasificación de las arcillas.
Quizá te estás preguntando por qué
le damos tanta importancia a las arcillas, si éste es un
archivo acerca
del vidrio. Lo que sucede es que queremos enseñarte y
convencerte de que la arcilla es como tierra, como
arena, y que de ella se obtienen los vidrios. Cuesta trabajo
imaginarlo, verdad? Piensa en la sorpresa que se llevó
el hombre
primitivo cuando lo descubrió. Puso a calentar tierra y
ésta se empezó a poner dura hasta que se
transformó en un vidrio. Suena como magia. Hoy sabemos que
a medida que la temperatura de tratamiento de la arcilla aumenta
más allá del rojo vivo, se produce un
endurecimiento, seguido de una compactación y finalmente
de una transformación de la arcilla en vidrio. Durante la
vitrificación se produce una considerable
contracción, debida a la disminución del
tamaño de las partículas y a una
reestructuración de las moléculas dentro de la
matriz
vítrea. Pero, de qué están formadas las
arcillas que les permite hacer todo eso? Las arcillas son
silicoaluminatos complejos. Un silicoaluminato es un compuesto
hecho con silicio y aluminio, que se forma cuando la
sílice modifica su superficie por la interacción
con iones aluminato, intercambiando iones
Si(OH)4- por iones
Al(OH)4-, como se ilustra en la figura 12.
Se pueden intercambiar unos por otros porque son muy parecidos
entre sí. El A1(OH)4- tiene una
carga negativa y cuatro grupos OH, igual que el
Si(OH)4-. Además, el silicio y el
aluminio son de un tamaño similar. Con el tiempo estos
compuestos reaccionan y forman sales solubles con los iones
alcalinos (Na, Li, y K) y alcalinotйrreos (Be, Mg y Ca),
cambiando así la estructura de
los silicoaluminatos originales. El aluminio puede estar rodeado
por 4 o 6 átomos de oxígeno, y puede tener carga +3 o +4.
Imaginemos un silicato donde uno de los бtomos de
Si+4 estб sustituido por un ion
Al+3.
Figura 12. Estructura del silicoaluminato en una
arcilla.
Como la carga global tiene que ser la misma y el silicio
tiene cuatro mientras que el aluminio tiene tres, se une un
K+1 o un Li+1 y resuelve el problema. En la
figura 13 aparece un dibujo de la
estructura de las arcillas con y sin metales. En la
figura 13(a) vemos que hay dos tipos diferentes de capas. En la
parte de abajo encontramos una capa de silicio, en medio una de
aluminio y a continuación otra de silicio, con sus
respectivos oxígenos cada una, por supuesto. Es claro que
el aluminio cambia la forma de la arcilla. En la figura 13(b) la
situación es similar, salvo que en ésta se indica
la posición que toman los átomos de potasio (K). Si
seguimos buscando diferencias, veremos que en la arcilla que
carece de metales (figura 13(a)) aparecen moléculas de
agua (H2O) entre capas de silicio. Por eso se dice que
todos estos minerales tienen
la propiedad de
absorber agua, lo que también contribuye a que las
estructuras
sean más anchas porque, como puedes ver, la de la figura
13(a) mide entre 9.6 y 21.4 Å, dependiendo de la cantidad
de agua que haya absorbido, mientras que la de la figura 13(b)
mide 10 Å. Estos cambios en la estructura de la arcilla son
la base de su naturaleza caprichosa.
Figura 13. Estructura cristalina de arcillas. a) Sin
metales alcalinos (montmorillonita). b) Con metales alcalinos y
alcalinotйrreos (illita).
En la sílice, la unidad estructural fundamental
es un tetraedro de SiO4, es decir, un átomo de
silicio rodeado siempre por cuatro átomos de
oxígeno (figura 14). Las fuerzas que mantienen unidos a
estos átomos comprenden enlaces iónicos y
covalentes, lo cual provoca que la fuerza del
enlace sea muy grande. Si pensamos en tetraedros de sílice
juntos, unos rodeando a otros, tendríamos una
combinación de tetraedros de sílice (con sus
respectivos oxígenos) orientados al azar. En un cristal
como el de la figura 15(a) los átomos siguen un
patrón estricto de orientación que se repite n
veces, siempre de la misma manera. En un vidrio, los enlaces
Si-O-Si no tienen una orientación determinada (figura 15
(b))s; la distancia de separación entre los
бtomos de Si y O no es homogйnea, las
unidades tetraйdricas no se repiten con regularidad y el
compuesto estб desordenado. A esta ъltima se le
conoce como sнlice amorfa, mientras que a la
ordenada se le conoce como sílice cristalina, y ambas se
utilizan en la fabricación del vidrio. El cuarzo (figura
16), es un ejemplo de sílice cristalina muy empleada en
esta manufactura.
Figura 14. Tetraedro de silicio rodeado de cuatro átomos
de oxígeno.
Figura 15.
Representaciуn grбfica de las diferencias
estructurales entre un cristal (a) y un vidrio
(b).
Figura 16. Estructura cristalina regular de cuarzo.
Con las arcillas se hacen los vidrios, y como existe una
gran variedad, el vidrio que obtengamos dependerá de la
arcilla que escojamos, razón por la cual se necesita
conocer muy bien las materias primas. Esto lo saben los
señores vidrieros, y por eso han aprendido que la
caolinita (figura 17) es el grupo de
minerales de arcilla más sencillo, su estructura
básica se compone de átomos de oxígeno
ordenados de tal manera que dan lugar a capas alternadas de
huecos tetraédricos, que se ocupan por átomos de
silicio y aluminio, y huecos octaédricos, ocupados por
átomos de aluminio, magnesio, hierro y
cinc.
Figura 17. Estructura de la caolinita.
También hay impurezas que ocupan sitios
intersticiales, o dicho de otra manera, tienen iones que
están mal acomodados. El efecto de las impurezas depende
de su naturaleza, de la proporción en que se encuentran,
del tamaño y de la forma de los granos de la arcilla, y de
las condiciones de reacción, incluyendo la temperatura
alcanzada, la duración del calentamiento y los efectos de
algunas otras sustancias presentes. Cuando estas impurezas son
compuestos de hierro, por ejemplo, el color de la arcilla cambia,
y aparecen eflorescencias de colores en la
superficie del material seco y manchas negras o grises.
También se modifican las propiedades refractarias. El
óxido férrico es altamente refractario cuando se
encuentra en una atmósfera oxidante;
en una reductora actúa como fundente. La diferencia entre
las dos situaciones es que en la primera el hierro pierde
electrones, mientras que en la segunda los gana. Esta disparidad
puede cambiar radicalmente las propiedades de la materia prima
necesaria para hacer un vidrio. Las impurezas nos pueden ayudar a
su manufactura, lo importante es saberlas escoger y
manejar.
Desde que el hombre primitivo descubrió el
vidrio, su fabricación ha cambiado poco, y ha dependido en
gran medida de la infraestructura disponible para la
fusión de las materias primas. Antiguamente se utilizaban
crisoles con capacidad de pocas toneladas (hoy en día se
siguen usando para elaborar vidrios especiales). En las grandes
fábricas modernas se utiliza el llamado horno tanque, que
consiste en un gran tanque cerrado, hecho con los mejores
materiales refractarios. El combustible (gas o petróleo)
se quema dentro del tanque, produce enormes llamas que pasan
sobre la superficie de vidrio fundido y sobre las materias primas
flotantes aún no fundidas. Los hornos tanque más
usuales son continuos, lo que quiere decir que las materias
primas que se introducen por el extremo de fusión salen
con la misma rapidez por el lado opuesto en forma de vidrio
fundido, para despuйs pasar a las
mбquinas que le dan forma. Existen hornos continuos muy
grandes, con una capacidad total de 450 toneladas y una
producciуn diaria de vidrio de
250 toneladas. Las altas temperaturas con las que trabajan estos
hornos (alrededor de 1 500єC) requieren sistemas de
caldeo regenerativos para recuperar parte del calor.
Cuando el vidrio sale del tanque de fusión se
enfría y se endurece rápidamente. En los pocos
segundos que permanece a una temperatura entre el rojo amarillo y
el rojo naranja se trabaja de muchas formas para darle diferentes
aspectos. Se puede prensar, soplar, estirar y laminar. El vidrio
frío puede volverse a calentar y trabajarse repetidas
veces con la misma facilidad aplicando el mismo método. Es
importante evitar que el vidrio caliente y blando permanezca a la
intemperie demasiado tiempo, porque se puede
cristalizar.
 En la
En la
producción a gran escala,
inmediatamente despuйs de que se le ha dado
forma a un articulo de vidrio, йste es transportado hasta
un horno de recocido continuo, en el cual se vuelve a calentar a
la temperatura apropiada. Con esto se evitan tensiones dentro del
material vítreo. Posteriormente se somete a
un enfriamiento lento y controlado. Despuйs de salir del
horno de cocido, cada articulo es inspeccionado, embalado y, si
es necesario, se somete a operaciones de
acabado. En la figura 18 se muestra un
diagrama del
proceso de fabricación del vidrio. La materia prima
se pone en el tanque de fusión. Una vez fundida se le da
forma para despuйs recocerla. Se puede ver que la
temperatura de recocido es relativamente baja comparada con la de
fusión, y que el vidrio roto de desecho se puede volver a
utilizar cuantas veces se desee.
Vidrio decorado
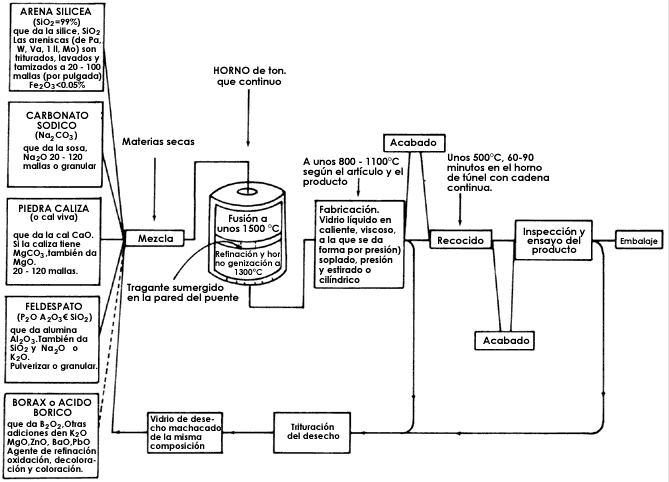
Figura 18. Diagrama para la fabricación de
vidrio.
Es importante destacar que el proceso de
fabricación es prácticamente el mismo para todos
los tipos, y lo que cambia de un ejemplar a otro es el material.
Todos ellos tienen en mayor o menor proporción
бtomos de silicio, que es uno de los elementos
de la tabla periуdica que mбs se parece al carbono.
Esto resulta interesante si pensamos que el carbono
es la base fundamental de la vida en nuestro planeta. Si son tan
parecidos, por qué no existe vida en la Tierra basada en
la química del silicio?, y por qué no podemos
utilizar el carbono para fabricar vidrio? La razón radica
en la gran facilidad que tiene el silicio para formar compuestos
con el oxigeno,
evitando con esto las largas cadenas que serían
equivalentes a las del carbono, y que son importantes en la
química de la vida. Es precisamente esta afinidad con el
oxigeno lo que lo hace útil e indispensable en la
formación del vidrio.
La sílice se funde a temperaturas muy altas para
obtener una masa vítrea. Dado que este vidrio tiene un
punto de fusión muy alto y no se contrae ni se dilata
demasiado con el cambio de
temperatura, es muy apropiado para aparatos de laboratorio y
para los objetos que han de someterse a grandes variaciones
térmicas, como los espejos de los telescopios. El vidrio
es mal conductor tanto del calor como de la electricidad, por
lo que suele utilizarse como aislante eléctrico y
térmico. Para elaborar la mayor parte de los vidrios se
combina la sílice con diferentes proporciones de otras
materias primas. Los fundentes alcalinos, normalmente carbonato
de sodio o de potasio, hacen que descienda la temperatura
requerida para la fusión y la viscosidad de la
sílice. La piedra caliza o la dolomita (carbonato de
calcio y magnesio) actúan como estabilizantes en el
horneado. Si se añaden otros ingredientes, como el plomo y
el bórax, se confiere al vidrio propiedades físicas
determinadas.
5. Vidrio soluble y vidrio
sodocálcico.-
El vidrio con gran contenido sódico, que puede
disolverse en agua convirtiéndose en un fluido espeso, es
conocido como vidrio soluble y se emplea como material
ignífugo y cemento de
sellado. La mayor parte del vidrio que se produce lleva como
álcalis sosa y cal y se utiliza para hacer botellas,
vajillas, bombillas, focos, ventanas y lunas.
El vidrio fino que se utiliza para vajillas y se conoce
como cristal es el resultado de fórmulas que combinan
sílice y potasio con óxido de plomo. El vidrio al
plomo es pesado y presenta un elevado índice de
refracción a la luz, lo que le
convierte en un material apropiado para la fabricación de
lentes y prismas, así como para joyas de imitación.
Dado que el plomo absorbe las radiaciones de alta energía,
en las instalaciones nucleares se utilizan vidrios al plomo para
la protección de los trabajadores.
Vidrio cuya composición presenta un predominancia
de bórax, además de sílice y álcali.
De larga durabilidad y muy resistente a los elementos
químicos y al fuego, se usa como material de cocina,
laboratorio y como equipo para procesos
químicos.
Las impurezas en la materia prima afectan a la
coloración del vidrio. Para obtener una sustancia
transparente e incolora, los fabricantes le añaden
manganeso, que contrarresta los efectos de las coloraciones
verdosas o amarillentas producidas por los óxidos de
hierro. El vidrio puede colorearse utilizando óxidos
metálicos, sulfuros o seleniuros. Otros colorantes
podrían dispersarse en partículas
microscópicas.
Entre los componentes típicos del vidrio
están los residuos de vidrio de composición
similar, que potencian su fusión y homogeneización.
A menudo se añaden elementos de afino, como
arsénico o antimonio, para desprender pequeñas
burbujas durante la fusión.
Según su composición, algunos vidrios
pueden fundir a temperaturas de sólo 500 °C; en
cambio, otros necesitan 1.650 ºC. La resistencia a la
tracción, que suele estar entre los 3.000 y 5.500 N/cm2,
puede llegar a los 70.000 N/cm2 si el vidrio recibe un
tratamiento especial. La densidad relativa
(densidad con respecto al agua) va de 2 a 8, es decir, el vidrio
puede ser más ligero que el aluminio o más pesado
que el acero. Las
propiedades ópticas y eléctricas también
pueden variar mucho.
Después de una cuidadosa medida y
preparación, las materias primas se mezclan y se someten a
una fusión inicial antes de aplicarles todo el calor
necesario para la vitrificación. En el pasado, la
fusión se efectuaba en recipientes de arcilla (barro) que
se calentaban en hornos alimentados con madera o carbón.
Todavía hoy se utilizan recipientes de arcilla
refractaria, que contienen entre 0,5 y 1,5 toneladas de vidrio,
cuando se necesitan cantidades relativamente pequeñas de
vidrio para trabajarlo a mano. En las industrias
modernas, la mayor parte del vidrio se funde en grandes calderos,
introducidos por primera vez en 1872. Estos calderos pueden
contener más de 1.000 toneladas de vidrio y se calientan
con gas, fuel-oil o electricidad. Las materias primas se
introducen de forma continua por una abertura situada en un
extremo del caldero y el vidrio fundido, afinado y templado, sale
por el otro extremo. En unos grandes crisoles o cámaras de
retención, el vidrio fundido se lleva a la temperatura a
la que puede ser trabajado y, a continuación, la masa
vítrea se transfiere a las máquinas
de moldeo.
Fabricación de vidrio
El vidrio se fabrica a partir de una mezcla compleja de
compuestos vitrificantes, como sílice, fundentes, como los
álcalis, y estabilizantes, como la cal. Estas materias
primas se cargan en el horno de cubeta (de producción
continua) por medio de una tolva. El horno se calienta con
quemadores de gas o petróleo. La llama debe alcanzar una
temperatura suficiente, y para ello el aire de combustión
se calienta en unos recuperadores construidos con ladrillos
refractarios antes de que llegue a los quemadores. El horno tiene
dos recuperadores cuyas funciones cambian cada veinte minutos:
uno se calienta por contacto con los gases ardientes mientras el
otro proporciona el calor acumulado al aire de combustión.
La mezcla se funde (zona de fusión) a unos
1.500 °C y avanza hacia la zona de enfriamiento, donde
tiene lugar el recocido. En el otro extremo del horno se alcanza
una temperatura de 1.200 a 800 °C. Al vidrio así
obtenido se le da forma por laminación (como en el
esquema) o por otro método.

Los principales métodos
empleados para moldear el vidrio son el colado, el soplado, el
prensado, el estirado y el laminado. Todos estos procesos son
antiguos, pero han sufrido modificaciones para poder producir
vidrio con fines industriales. Por ejemplo, se han desarrollado
procesos de colado por centrifugado en los que el vidrio se
fuerza contra las paredes de un molde que gira
rápidamente, lo que permite obtener formas precisas de
poco peso, como tubos de televisión. También se han
desarrollado máquinas automáticas para soplar el
vidrio.
Vidrio soplado
Fabricación artesanal de recipientes de vidrio soplado. A
la izquierda se aprecia una silla con un soporte para la
caña de soplar. Conseguida la forma en bruto, se pellizca
el material con unas pinzas para dar la forma final al vidrio
fundido.
Es posible añadir tensiones de modo artificial
para dar resistencia a un artículo de vidrio. Como el
vidrio se rompe como resultado de esfuerzos de tracción
que se originan con un mínimo arañazo de la
superficie, la compresión de ésta aumenta el
esfuerzo de tracción que puede soportar el vidrio antes de
que se produzca la ruptura. Un método llamado temple
térmico comprime la superficie calentando el vidrio casi
hasta el punto de reblandecimiento y enfriándolo
rápidamente con un chorro de aire o por inmersión
en un líquido. La superficie se endurece de inmediato, y
la posterior contracción del interior del vidrio, que se
enfría con más lentitud, tira de ella y la
comprime. Con este método pueden obtenerse compresiones de
superficie de hasta 24.000 N/cm2 en piezas gruesas de vidrio.
También se han desarrollado métodos químicos
de reforzamiento en los que se altera la composición o la
estructura de la superficie del vidrio mediante intercambio
iónico. Este método permite alcanzar una
resistencia superior a los 70.000 N/cm2.
14. Tipos de vidrio
comercial.-
La amplia gama de aplicaciones del vidrio ha hecho que
se desarrollen numerosos tipos distintos.
Vidrio de ventana.-
El vidrio de ventana, que ya se empleaba en el siglo I d.C., se
fabricaba utilizando moldes o soplando cilindros huecos que se
cortaban y aplastaban para formar láminas. En el proceso
de corona, técnica posterior, se soplaba un trozo de
vidrio dándole forma de globo aplastado o corona. La
varilla se fijaba al lado plano y se retiraba el tubo de soplado.
La corona volvía a calentarse y se hacía girar con
la varilla; el agujero dejado por el tubo se hacía
más grande y el disco acababa formando una gran
lámina circular. La varilla se partía, lo que
dejaba una marca. En la
actualidad, casi todo el vidrio de ventana se fabrica de forma
mecánica estirándolo desde una piscina de vidrio
fundido. En el proceso de Foucault, la
lámina de vidrio se estira a través de un bloque
refractario ranurado sumergido en la superficie de la piscina de
este material y se lleva a un horno vertical de recocido, de
donde sale para ser cortado en hojas.
Vidrio de placa.-
El vidrio de ventana normal producido por estiramiento
no tiene un espesor uniforme, debido a la naturaleza del proceso
de fabricación. Las variaciones de espesor distorsionan la
imagen de los
objetos vistos a través de una hoja de ese
vidrio.
El método tradicional de eliminar esos defectos
ha sido emplear vidrio laminado bruñido y pulimentado,
conocido como vidrio de placa. Éste se produjo por primera
vez en Saint Gobain (Francia) en
1668, vertiendo vidrio en una mesa de hierro y aplanándolo
con un rodillo. Después del recocido, la lámina se
bruñía y pulimentaba por ambos lados. Hoy, el
vidrio de placa se fabrica pasando el material vítreo de
forma continua entre dobles rodillos situados en el extremo de un
crisol que contiene el material fundido. Después de
recocer la lámina en bruto, ambas caras son acabadas de
forma continua y simultánea.
En la actualidad, el bruñido y el pulimentado
están siendo sustituidos por el proceso de vidrio
flotante, más barato. En este proceso se forman
superficies planas en ambas caras haciendo flotar una capa
continua de vidrio sobre un baño de estaño fundido.
La temperatura es tan alta que las imperfecciones superficiales
se eliminan por el flujo del vidrio. La temperatura se hace
descender poco a poco a medida que el material avanza por el
baño de estaño y, al llegar al extremo, el vidrio
pasa por un largo horno de recocido.
En arquitectura se
emplea vidrio laminado sin pulir, a menudo con superficies
figurativas producidas por dibujos
grabados en los rodillos. El vidrio de rejilla, que se fabrica
introduciendo tela metálica en el vidrio fundido antes de
pasar por los rodillos, no se astilla al recibir un golpe. El
vidrio de seguridad, como
el utilizado en los parabrisas de los automóviles o en las
gafas de seguridad, se obtiene tras la colocación de una
lámina de plástico
transparente (polivinilbutiral) entre dos láminas finas de
vidrio de placa. El plástico se adhiere al vidrio y
mantiene fijas las esquirlas incluso después de un fuerte
impacto
Botellas y recipientes.-
Las botellas, tarros y otros recipientes de vidrio se fabrican
mediante un proceso automático que combina el prensado
(para formar el extremo abierto) y el soplado (para formar el
cuerpo hueco del recipiente). En una máquina típica
para soplar botellas, se deja caer vidrio fundido en un molde
estrecho invertido y se presiona con un chorro de aire hacia el
extremo inferior del molde, que corresponde al cuello de la
botella terminada. Después, un desviador desciende sobre
la parte superior del molde, y un chorro de aire que viene desde
abajo y pasa por el cuello da la primera forma a la botella. Esta
botella a medio formar se sujeta por el cuello, se invierte y se
pasa a un segundo molde de acabado, en la que otro chorro de aire
le da sus dimensiones finales. En otro tipo de máquina que
se utiliza para recipientes de boca ancha, se prensa el vidrio
en un molde con un pistón antes de soplarlo en un molde de
acabado. Los tarros de poco fondo, como los empleados para
cosméticos, son prensados sin más.
Vidrio óptico.-
La mayoría de las lentes que se utilizan en gafas
(anteojos), microscopios, telescopios, cámaras y otros
instrumentos ópticos se fabrican con vidrio óptico.
Éste se diferencia de los demás vidrios por su
forma de desviar (refractar) la luz. La fabricación de
vidrio óptico es un proceso delicado y exigente. Las
materias primas deben tener una gran pureza, y hay que tener
mucho cuidado para que no se introduzcan imperfecciones en el
proceso de fabricación. Pequeñas burbujas de aire o
inclusiones de materia no vitrificada pueden provocar
distorsiones en la superficie de la lente. Las llamadas cuerdas,
estrías causadas por la falta de homogeneidad
química del vidrio, también pueden causar
distorsiones importantes, y las tensiones en el vidrio debidas a
un recocido imperfecto afectan también a las cualidades
ópticas.
En la antigüedad, el vidrio óptico se
fundía en crisoles durante periodos prolongados,
removiéndolo constantemente con una varilla refractaria.
Después de un largo recocido, se partía en varios
fragmentos; los mejores volvían a ser triturados,
recalentados y prensados con la forma deseada. En los
últimos años se ha adoptado un método para
la fabricación continua de vidrio en tanques revestidos de
platino, con agitadores en las cámaras cilíndricas
de los extremos (llamadas homogeneizadores). Este proceso produce
cantidades mayores de vidrio óptico, con menor coste y
mayor calidad que el
método anterior. Para las lentes sencillas se usa cada vez
más el plástico en lugar del vidrio. Aunque no es
tan duradero ni resistente al rayado como el vidrio, es fuerte y
ligero y puede absorber tintes
Vidrio fotosensible.-
En el vidrio fotosensible, los iones de oro o plata del material
responden a la acción de la luz, de forma similar a lo que
ocurre en una película fotográfica. Este vidrio se
utiliza en procesos de impresión y reproducción, y su tratamiento
térmico tras la exposición
a la luz produce cambios permanentes.
El vidrio fotocromático se oscurece al ser
expuesto a la luz tras lo cual recupera su claridad original.
Este comportamiento
se debe a la acción de la luz sobre cristales diminutos de
cloruro de plata o bromuro de plata distribuidos por todo el
vidrio. Es muy utilizado en lentes de gafas o anteojos y en
electrónica.
Vitrocerámica.-
En los vidrios que contienen determinados metales se produce una
cristalización localizada al ser expuestos a radiación
ultravioleta. Si se calientan a temperaturas elevadas, estos
vidrios se convierten en vitrocerámica, que tiene una
resistencia mecánica y unas propiedades de aislamiento
eléctrico superiores a las del vidrio ordinario. Este tipo
de cerámica se utiliza en la actualidad en
utensilios de cocina, conos frontales de cohetes o ladrillos
termorresistentes para recubrir naves espaciales. Otros vidrios
que contienen metales o aleaciones
pueden magnetizarse, son resistentes y flexibles y resultan muy
útiles para transformadores
eléctricos de alta eficiencia
Fibra de vidrio.-
Es posible producir fibras de vidrio —que pueden tejerse
como las fibras textiles— estirando vidrio fundido hasta
diámetros inferiores a una centésima de
milímetro. Se pueden producir tanto hilos multifilamento
largos y continuos como fibras cortas de 25 o 30
centímetros de largo.
Una vez tejida para formar telas, la fibra de vidrio
resulta ser un excelente material para cortinas y
tapicería debido a su estabilidad química, solidez
y resistencia al fuego y al agua. Los tejidos de fibra
de vidrio, sola o en combinación con resinas, constituyen
un aislamiento eléctrico excelente. Impregnando fibras de
vidrio con plásticos
se forma un tipo compuesto que combina la solidez y estabilidad
química del vidrio con la resistencia al impacto del
plástico. Otras fibras de vidrio muy útiles son las
empleadas para transmitir señales ópticas en
comunicaciones
informáticas y telefónicas mediante la nueva
tecnología de la fibra
óptica, en rápido crecimiento.
Otros tipos de vidrio.-
Los paveses de vidrio son bloques de construcción huecos, con nervios o dibujos
en los lados, que se pueden unir con argamasa y utilizarse en
paredes exteriores o tabiques internos.
La espuma de vidrio, empleada en flotadores o como
aislante, se fabrica añadiendo un agente espumante al
vidrio triturado y calentando la mezcla hasta el punto de
reblandecimiento. El agente espumante libera un gas que produce
una multitud de pequeñas burbujas dentro del
vidrio.
En la década de 1950 se desarrollaron fibras
ópticas que han encontrado muchas aplicaciones en la ciencia, la
medicina y la
industria. Si se colocan de forma paralela fibras de vidrio de
alto índice de refracción separadas por capas
delgadas de vidrio de bajo índice de refracción, es
posible transmitir imágenes a
través de las fibras. Los fibroscopios, que contienen
muchos haces flexibles de estas fibras, pueden transmitir
imágenes a través de ángulos muy cerrados,
lo que facilita la inspección de zonas que suelen ser
inaccesibles. Las aplicaciones de la fibra óptica
rígida, como lupas, reductores y pantallas también
mejoran la visión. Empleadas en combinación con
láseres, las fibras ópticas son hoy cruciales para
la telefonía de larga distancia y la
comunicación entre ordenadores (computadoras).
El vidrio láser es
vidrio dopado con un pequeño porcentaje de óxido de
neodimio, y es capaz de emitir luz láser si se monta en un
dispositivo adecuado y se ‘bombea’ con luz ordinaria.
Está considerado como una buena fuente láser por la
relativa facilidad con que pueden obtenerse pedazos grandes y
homogéneos de este vidrio.
Los vidrios dobles son dos láminas de vidrio de placa o de
ventana selladas por los extremos, con un espacio de aire entre
ambas. Para su construcción pueden usarse varios tipos de
selladores y materiales de separación. Empleados en
ventanas, proporcionan un excelente aislamiento térmico y
no se empañan aunque haya humedad
En la década de 1980 se desarrolló en la Universidad de
Florida (Estados Unidos)
un método para fabricar grandes estructuras de vidrio sin
utilizar altas temperaturas. La técnica, denominada de
sol-gel, consiste en mezclar agua con un producto químico
como el tetrametoxisilano para fabricar un polímero de
óxido de silicio; un aditivo químico reduce la
velocidad del
proceso de condensación y permite que el polímero
se constituya uniformemente. Este método podría
resultar útil para fabricar formas grandes y complejas con
propiedades específicas.
Fórmula química:
Mg3Si4O10(OH)2
Clase:
Silicatos
Subclase:
Filosilicatos
Grupo:
Minerales arcillosos
Etimología: Deriva
probablemente del árabe "talk" nombre del
mineral.
Cristalografía:
Sistema y clase:
Monoclínico; 2/m
Grupo espacial: C2c
a = 5.27 Å, b = 9.12, c = 18.85 Å, b = 100º; Z =
4
Líneas de DRX(intensidades) d´s: 9.34(10) – 4.66(9)
– 3.12(10) – 2.48(7) – 1.870(4).
Propiedades físicas:
Color: | Verde pálido, blanco, negro, rosado y |
Raya: | Blanca o más clara que el color en sus |
Brillo: | Craso, céreo o sedoso. |
Dureza: | De 1 a 1.5 |
Densidad: | De 2.6 a 2.7g/cm3 |
Óptica: | Birrefringencia fuerte. |
Química: Contiene el 31,7% de MgO,
el 64,5% de SiO2 y el 4,8% de H2O. Puede
contener algo de Fe, Al, Ni, Co, Cr, Mn y Ca. Inatacable por los
ácidos.
Forma de presentarse: En masas
de tipo testáceo,
hojosas, o escamosas, untuosas al tacto, también en masas
granudas compactas o fibrosas o en grupos globulares o
estrellados. Las variedades masivas se conocen como
Esteatita.
Génesis:
| Hidrotermal formado a partir de rocas ultra |
| Por metasomatismo silíceo de |


El talco
Oferta y
demanda mundial del talco.-
1. Producción mundial.-
El espectro de usos finales del talco demanda una
multitud de grados, que no pueden ser satisfechos por una sola
fuente. Consecuentemente, 40 países contribuyen a la
producción mundial de alrededor 8,4 millones de toneladas
promedio de talco, pirofilita y esteatita. El nivel de
producción en el período 1993-1997 no ha sufrido
fuertes oscilaciones manteniendo un comportamiento medianamente
estable con un aumento entre ambos años del 2,4%.
La producción está dominada por China con una
participación del 30% y, en segundo lugar, por USA con el
12%. En importancia son seguidos por India,
Finlandia, Francia y Brasil cuyos
aportes rondan entre el 4 y 5% cada uno.
En Latinoamérica se encuentran como
productores de talco los siguientes países: Brasil,
Argentina,
Chile,
Colombia,
Venezuela,
Perú y Uruguay con
niveles inferiores a las 30.000 t/año a excepción
de Brasil.
Dado que el talco ocurre tanto puro como asociado a otros tantos
minerales como clorita, magnesita y serpentinita entre otros, se
puede destacar que en Australia, China y USA (Montana) se
encuentra talco puro; en Francia, Austria e Italia asociado a
clorita; en Canadá (Quebec y Ontario) y Finlandia ocurre
con magnesita y, por último, en Suiza y USA (New York)
está con tremolita.
Algunos países han ganado una buena
reputación en una o más industrias, como los talcos
de Francia, China y Australia en cosméticos y el talco de
New York en cerámicas, y sus productos recorren largas
distancias hasta llegar a diversos centros de consumo
Tabla I : Producción mundial (1993 – 1997)
(toneladas)
Países | 1993 | 1994 | 1995 | 1996 | 1997 |
China | 2.700.000 | 2.400.000 | 2.400.000 | 2.400.000 | 2.350.000 |
USA | 968.000 | 935.000 | 1.060.000 | 994.000 | 1.050.000 |
Italia | 140.939 | 138.416 | 159.106 | 132.647 | 141.000 |
Corea | 180.000 | 180.000 | 180.000 | 180.000 | 180.000 |
India | 385.121 | 398.006 | 439.509 | 472.001 | 470.000 |
Brasil | 345.843 | 356.919 | 254.919 | 250.000 | S/d |
Finlandia | 347.859 | 395.297 | 405.025 | 345.282 | 400.000 |
Australia | 172.273 | 154.000 | 125.701 | 176.000 | 190.000 |
Austria | 136.640 | 130.602 | 131.614 | 129.748 | 141.984 |
Francia | 299.900 | 306.400 | 322.400 | 349.300 | 334.800 |
Resto (*) | 2.523.425 | 2.505.360 | 2.621.726 | 2.571.022 | 3.242.216 |
Total | 8.200.000 | 7.900.000 | 8.100.000 | 8.000.000 | 8.500.000 |
Fuente: World Mineral Statistics 1988/92
– 1991/95
(*) Incluye, en algunos casos, producción de
pirofilita y esteatita
2. Países importadores.-
Entre los principales países importadores del talco se
encuentran Japón
con cantidades que rondan las 600.000 toneladas anuales seguido
por Corea con un promedio de 290.000 t./año y Alemania con
235.000t./año.
Tabla II : Importación mundial (1993 – 1997)
(toneladas)
Países | 1993 | 1994 | 1995 | 1996 | 1997 |
Japón | 588.777 | 601.793 | 720.901 | 567.721 | 579.930 |
Alemania | 239.743 | 237.139 | 241.536 | 226.138 | 228.450 |
Taiwán | 151.026 | 180.200 | 165.906 | 136.799 | 132.001 |
USA | 97.525 | 152.475 | 142.886 | 179.738 | 115.166 |
México | 103.017 | 118.376 | 100.216 | 112.872 | — |
Corea | 264.258 | 310.952 | 390.567 | 276.323 | 210.047 |
Indonesia | 59.610 | 58.327 | 88.146 | 109.550 | 88.156 |
Reino Unido | 127.484 | 69.972 | 68.839 | 73.084 | 83.013 |
Países Bajos | 73.020 | 163.585 | 141.160 | 134.954 | 81.171 |
Bélgica – Luxemburgo | 113.170 | 60.385 | 72.139 | 73.415 | 96.181 |
Fuente: World Mineral Statistics 1993-1997
3. Países exportadores.-
China es el principal país exportador de talco con un
promedio de 1,2 millones de toneladas anuales siendo una
importante fuente de abastecimiento del mercado
asiático. En segundo lugar, se ubica la República
de Corea con 243.000 t/año, principalmente de pirofilita,
seguido por Estados Unidos, Finlandia, Francia, Australia y
Austria cuya colocación de talco en los mercados externos
es inferiores a 200.000 t/año.
Tabla III : Exportación mundial (1993 – 1997)
(toneladas)
Países | 1993 | 1994 | 1995 | 1996 | 1997 |
China | 1.063.926 | 1.243.396 | 1.600.326 | 1.023.901 | 1.021.001 |
Corea | 224.399 | 248.907 | 256.067 | 228.808 | 255.597 |
USA | 145.315 | 165.180 | 191.585 | 198.969 | 188.902 |
Francia | 128.622 | 144.106 | 160.024 | 176.799 | 209.299 |
Austria | 125.146 | 129.944 | 142.245 | 145.925 | 146.131 |
Finlandia | 111.700 | 174.400 | 186.500 | 168.000 | S/d |
Australia | 119.830 | 152.295 | 133.046 | 182.297 | 143.226 |
Fuente: World Mineral Statistics, 1993-1999
4. Consumo
mundial.-
Los datos sobre consumo mundial de talco y pirofilita por
región que se presentan a continuación son
estimativos.
Tabla IV : Consumo estimado por región (1994)
(miles toneladas)
Región | Talco | Pirofilita | ||
Miles de toneladas | % | Miles de toneladas | % | |
América del Norte | 950 | 13 | 100 | 4 |
Sudamérica | 690 | 12 | 250 | 10 |
Europa Occidental | 1.185 | 18 | 25 | 1 |
Europa del Este | 350 | 9 | 15 | 1 |
Asia | 3.400 | 47 | 2.100 | 84 |
África y Oceanía | 65 | 1 | 10 | — |
Total | 6.640 | 100 | 2.500 | 100 |
Fuente: Roskill, The Economics of Talc
La distribución del consumo de talco presenta
algunas diferencias con la pirofilita. Si bien Asia
continúa siendo el principal consumidor su
participación es menor (47%), y a excepción de
Oceanía y
África, las restantes regiones tienen una
participación que ronda en un promedio del 13%.
Consumo Mundial por uso final.-
La principal característica del consumo mundial de los
productos de talco procesados es la existencia de diferentes
patrones de consumo observado en las regiones geográficas.
En Asia y Europa Oriental
la industria del papel es responsable de más de la mitad
del talco consumido, mientras que en Norteamérica y
Sudamérica el consumo por esta industria es menor al 20%
del total. Se estima que en Sudamérica más del 50%
del talco consumido se destina a la industria de la
cerámica, en Norteamérica esta industria consume
menos del 20% y en Asia alrededor del 15%.
En cuanto al consumo mundial de productos de talco
según su uso final, seguidamente se muestra a modo de
orientación, el consumo por uso y continente, expresado en
miles de toneladas (1994).
El principal uso del talco a escala mundial es para
aplicaciones en papel. Dicho uso demanda cerca del 42,8% del
total seguido por la industria de cerámicas con un 20%. El
resto de las aplicaciones no supera el 10% del consumo total. Es
importante destacar que la distribución porcentual en los
diversos usos varía de acuerdo al continente al que se
refiera
Tabla V : Consumo mundial por región y uso final,
1994 (miles de toneladas)
Aplicación | América del Norte | América del Sur | Europa Occidental | Europa Oriental | Africa y Oceanía | Asia | Total |
Papel | 165 | 85 | 475 | 175 | 20 | 1.900 | 2.820 |
Plásticos | 65 | 30 | 150 | 30 | 15 | 310 | 600 |
Pinturas | 155 | 45 | 140 | 30 | 5 | 170 | 545 |
Cerámicas | 285 | 450 | 75 | 40 | 10 | 500 | 1.360 |
Cosméticos | 45 | 10 | 30 | 10 | 2 | 35 | 132 |
Agroquímicos | 13 | 10 | 130 | 15 | 3 | 55 | 226 |
Techado | 65 | 50 | 80 | 40 | 6 | 100 | 341 |
Caucho | 25 | 5 | 10 | 2 | 30 | 67 | |
Otros | 137 | 5 | 95 | 8 | 4 | 300 | 549 |
Total | 950 | 690 | 1.185 | 350 | 65 | 3.400 | 6.640 |
Fuente: Roskill, The Economics of Talc,
1996
MERCOSUR, Chile y Bolivia.-
1. BRASIL.-
Las reservas de talco en Brasil están localizadas en Minas
Gerais (49%), Bahía (30%), Paraná (15%), San Pablo
(4%), y situándose el resto en Río Grande do Sul,
Goias y Ceara. Las reservas de pirofilita se concentran en minas
Gerais (99,96%), Bahía, Paraná y San Pablo
(solamente reservas inferidas).
Las reservas totales alcanzan 178 millones de toneladas con una
participación de Brasil del 19% en las estimadas
mundialmente siendo precedidas por Estados Unidos (57%) y
Japón (21%).
Producción:
En 1998. la producción estimada de talco fue de 289.000t y
de pirofilita de 161.000t sumando 450.000t, con un nivel
constante con relación a 1997. Los Estados de
Paraná (50%), Bahía (25%), San Pablo (24%) y Minas
Gerais (1%) participan con el total de producción de
talco. Se destacan, en 1998, la firmas Costalco Mineracao
Indústria y Comércio Ltda, Magnesita SA, Sao Judas
Ltda, Mineradora Conventos SA e Itajara Minerios Ltda con una
contribución del 55% de la producción de
talco.
Importación:
En 1998, fueron importadas 10.590t de talco equivalentes a
US$3.025.648 con un incremento del 11% con respecto al volumen importado
en el año anterior. El precio
promedio de importación fue de US$FOB0,28/kg y el
principal país vendedor fue Estados Unidos con más
del 95% del total.
Exportación:
Las exportaciones de
talco totalizaron 3.925t con un valor de
US$1.060.896, estas cifras muestran una caída con respecto
a 1997 del 25% en volumen. El mercado al cual fueron destinadas
las exportaciones brasileñas lo constituyeron: Argentina
(61%), Uruguay y Paraguay (10,2%
c/u), Venezuela (6,6%), Alemania (4,9%) y Estados Unidos
(2,8%).
Consumo:
El talco y la pirofilita poseen aplicaciones en diversos sectores
industriales: cerámica, pisos, cerámica
artística y eléctrica, lozas y porcelanas,
refractarios, papel, fertilizantes e insumos agrícolas y
veterinarios, perfumería y cosmética, velas,
plásticos, industria de alimentos, minas
de papel, explosivos, esculturas, entre otros.
El consumo aparente nacional de 56.665t se mantuvo estable. Se
destacan como grandes consumidores la industria de productos
cerámicos (66%), química (8%), perfumería,
jabones y velas (4%), productos alimenticios (3%); los restantes
son la industria de materiales plásticos, papel,
farmacéutica y veterinaria, minas de
lápiz.
2. Paraguay.-
Producción:
En 1996, la producción de talco fue de 898,35 toneladas
correspondientes a talco de 1° 29,32t, talco de 2°
175,82t y talco de 3° 693,21t.
Comercio Exterior:
Las exportaciones de talco para 1996 totalizaron 36t equivalente
a U$S 18.400 con una caída del 25% con relación al
monto exportado durante 1995.
Las importaciones,
por su parte, registraron para el talco sin triturar ni
pulverizar 120t por un valor de 54.100 dólares, y para
talco triturado o pulverizado 282,4t equivalente a U$S 105.700
para 1996. Tales montos significaron un aumento del 53% con
relación a 1995.
3. Uruguay.-
No se registran datos de producción ni exportación.
Respecto a las importaciones de talco, en 1995 Paraguay
importó esteatita natural, talco, proveniente de Alemania
14 mil t, Argentina 1,8 mil t, Brasil 49 mil t e Italia 7 mil
t.
En 1996 no se registra intercambio comercial de dicho
mineral.
4. Chile.-
Producción:
El talco sufrió importantes cambios en el nivel de
producción en el transcurso de esta década para
alcanzar en 1996 un volumen total de 4.276 t. con un valor de U$S
341.000.
La Región V concentra el 55% del total producido con 2.351
t., el resto se distribuye en partes iguales entre la
Región IV y VII. En la tabla XLI se muestra la
producción de talco en el periodo 1990/96, expresada en
toneladas.
Tabla VI : Producción de Talco 1990-1996
(t.)
Años | Toneladas |
1990 | 898 |
1991 | 548 |
1992 | 1.493 |
1993 | 5.058 |
1994 | 5.351 |
1995 | 4.107 |
1996 | 4.276 |
Fuente: Anuario de la Minería de
Chile, 1996
Los principales usos a los cuales se destina el talco son la
industria del papel y del caucho, y para la fabricación de
pinturas y pesticidas.
Las principales empresas
productoras son:
Soc. Minera Godoy
Schwenger Ltda.
Mario Pizarro A.
Talco Eduardo
Martín A.
Comercio exterior:
No se obtuvieron datos detallados sobre el intercambio comercial
de talco.
El talco es uno de los principales productos exportados a
Perú. Durante estos últimos cuatro años se
ha observado una tendencia positiva, alcanzando en 1996 un valor
CIF de U$S 565.000.
5. Bolivia.-
No se registran datos de producción y comercio
exterior.
Nota:
Escala de dureza de Mohs.-
La dureza de un material determina su durabilidad. La escala de
Mohs se utiliza para evaluar la dureza relativa de una muestra al
realizar pruebas de
rayado sobre ella.
MINERAL | DUREZA | PRUEBA COMÚN |
Talco | 1 | Se raya con una uña |
Calcita | 3 | Se raya con una moneda de cobre |
Fluorita | 4 | Se raya con la hoja de un cuchillo o el cristal de |
Feldespato | 6 | Raya una hoja de cuchillo o el cristal de una |
Diamante | 10 | Raya todos los materiales comunes |
Autor:
Hugo Jesús Montenegro Ruiz